题目内容
7. 乙烯酮在一定条件下能与含活泼氢的化合物发生加成:它与下列试剂发生加成反应时所生成的产物不正确的是( )
乙烯酮在一定条件下能与含活泼氢的化合物发生加成:它与下列试剂发生加成反应时所生成的产物不正确的是( )| A. | 与HCl加成生成CH3COCl | B. | 与H2O加成生成CH3COOH | ||
| C. | 与CH3OH加成生成CH3COCH2OH | D. | 与CH3COOH加成生成(CH3CO)2O |
分析 依题中信息知:活性氢原子加到CH2=C=O中烃基碳上,其余部分加到羰基碳上,据此判断.
解答 解:依题中信息知:活性氢原子加到CH2=C=O中烃基碳上,其余部分加到羰基碳上.
A、乙烯酮(CH2=C=O)与HCl加成生成CH3COCl,故A正确;
B、乙烯酮(CH2=C=O)与H2O加成时得CH3COOH,故B正确;
C、乙烯酮(CH2=C=O)与CH3OH加成时得CH3COOCH3,故C错误;
D、乙烯酮(CH2=C=O)与CH3COOH加成时得CH3COOCOCH3,故D正确.
故选C.
点评 本题为信息给予题,考查学生根据题干提取有用信息能力,难度中等,清楚活性氢原子加到CH2=C=O中烃基碳上,其余部分加到羰基碳上是解题关键.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
17.下列有关两种微粒ZAX和ZA+1X+的叙述正确的是( )
| A. | 一定都是由质子、中子、电子组成的 | |
| B. | 化学性质几乎完全相同 | |
| C. | 核电荷数和核外电子数一定相等 | |
| D. | 质子数一定相同,质量数和中子数一定不相同 |
15.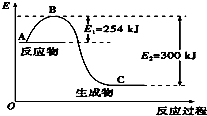 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,A代表的含义代表反应物的总能量A与C差值代表的含义代表反应热的大小.请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92KJ/mol.反应过程中加入正向催化剂,E1和E2变化情况变小(变大,变小,不变),△H变化情况不变(变大,变小,不变)假设此反应在密闭容器中反应过程中活化分子百分数变化情况变大(变大,变小,不变).
(2)若已知下列数据
试根据表中及图中数据计算N-H的键能为390kJ•mol-1.
(3)用NH3催化还原NOx还可以消除氮氧化物的污染.
例如:4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H1=-a kJ•mol-1 ①
N2(g)+O2(g)═2NO(g)△H2=-b kJ•mol-1 ②
若1mol NH3还原NO至N2,并生成水蒸气,则该反应过程中的反应热△H3=$\frac{(3b-a)}{4}$kJ•mol-1(用含a、b的式子表示).
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,A代表的含义代表反应物的总能量A与C差值代表的含义代表反应热的大小.请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92KJ/mol.反应过程中加入正向催化剂,E1和E2变化情况变小(变大,变小,不变),△H变化情况不变(变大,变小,不变)假设此反应在密闭容器中反应过程中活化分子百分数变化情况变大(变大,变小,不变).
(2)若已知下列数据
| 化学键 | H-H | N≡N |
| 键能/kJ•mol-1 | 435 | 943 |
(3)用NH3催化还原NOx还可以消除氮氧化物的污染.
例如:4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H1=-a kJ•mol-1 ①
N2(g)+O2(g)═2NO(g)△H2=-b kJ•mol-1 ②
若1mol NH3还原NO至N2,并生成水蒸气,则该反应过程中的反应热△H3=$\frac{(3b-a)}{4}$kJ•mol-1(用含a、b的式子表示).
2.前不久,我国科学家合成了三种新核素,其中一种是185Hf.下列关于18572Hf的叙述中正确的是( )
| A. | 该元素的原子序数是72 | B. | 该元素的原子序数是185 | ||
| C. | 该原子相对原子质量是185 | D. | 该元素是一种新元素 |
12.元素性质随原子序数的递增呈周期性变化的本质是( )
| A. | 原子核外电子排布呈现周期性变化 | |
| B. | 原子的电子层数增多 | |
| C. | 元素的相对原子质量逐渐增大,量变引起质变 | |
| D. | 原子半径呈周期性变化 |
19.难溶电解质AB2的饱和溶液中[A2+]=x mol•L-1,[B-]=y mol•L-1,则Ksp值为( )
| A. | 0.5xy2 | B. | xy | C. | xy2 | D. | 4xy2 |
16.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是( )
| A. | 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 | |
| C. | 根据同周期元素的电负性变化趋势,推出Ar的电负性比Cl大 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
17.居里夫人发现了放射性元素镭(${\;}_{88}^{226}$Ra),该元素含有的中子数为( )
| A. | 88 | B. | 138 | C. | 226 | D. | 314 |