题目内容
将等物质的量的A、B混合于2L密闭容器中发生如下反应:3A(g)+B(g)=xC(g)+2D(g)经5分钟后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5, C的平均反应速率是0.1mol/(L.min)求:
(1)此时A的浓度及反应开始前容器中A、B的物质的量分别为 、 、
(2)B的平均反应速率 。 (3)x= 。
(1) 0.75mol/L 3 3 (2) 0.05 mol/(L.min) (3) 2
解析:C的平均反应速率是0.1mol/(L.min),所以再反应过程生成的C是0.1mol/(L.min)×5min×2L=1.0mol。设反应前A、B的物质的量是a,则
3A(g) + B(g)=xC(g)+2D(g)
起始量(mol) a a 0 0
转化量(mol) 3/x 1/x 1 2/x
平衡量(mol) (a-3/x) (a-1/x) 1 2/x
所以2/x=0.5mol/L×2L,解得x=2.
又因为c(A):c(B)=3:5,所以(a-3/x)︰(a-1/x)=3:5,解得a=3.
即此时A的浓度是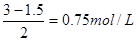 。
。
根据速率之比是相应的化学计量数之比可得B的平均反应速率为
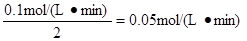

练习册系列答案
相关题目
 xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求: xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求: xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min).求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min).求: