题目内容
电浮选凝聚法处理酸性污水的工作原理如图所示。下列说法不正确的是
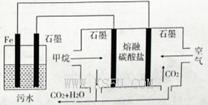

A.铁电极的电极反应式为: |
B.通人空气的石墨电极的电极反应式为 |
| C.若左池石墨电极产生44. 8L(标准状况)气体,则消耗氧气0. 5mol |
| D.为增强污水的导电能力,可向污水中加入适量工业用食盐 |
C
试题分析:在甲烷燃料电池中,通入甲烷的一极为原电池的负极,发生氧化反应,电极方程式为CH4+ 4CO32--8e-═5CO2+2H2O,通入空气(氧气)的一极为原电池的正极,发生还原反应,电极方程式为O2+ 2CO2+4e-=2CO32-,铁连接原电池的正极,为电解池的阳极,被氧化,发生Fe-2e-=Fe2+,阴极生成2H++ 2e-=H2↑,A.铁连接原电池的正极,为电解池的阳极,被氧化,电极反应为Fe-2e-=Fe2+,正确; B.甲烷的一极为原电池的负极,发生氧化反应,电极方程式为CH4+4CO32--8e-═5CO2+2H2O,故正确; C.n(H2) =2mol.则电子转移4mol。由于在同一个闭合回路中的电子转移数目相等,所以结合原电池的电极反应式可确定消耗氧气1mol.错误。D.加入的使导电能力增强的电解质必须是可溶于水的、显中性的盐,可用食盐,故正确;

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
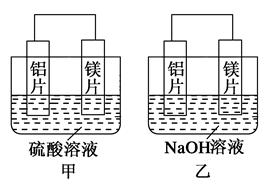
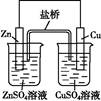
 3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( ) +4H2O+3e-
+4H2O+3e-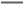 Fe(OH)3+5OH-
Fe(OH)3+5OH-
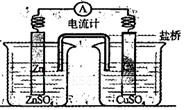
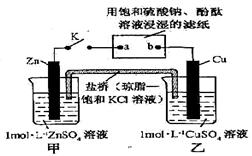
 电极上发生还原反应
电极上发生还原反应 a
a