题目内容
(4分)把足量的铁粉投入到100 mL 1.0 mol/L的盐酸中,充分反应后能得到标准状况下氢气的体积是多少?(要求有计算过程)
解:设反应后得到标况下H2的体积为xL
Fe + 2HCl = FeCl2 + H2
2 22.4
100×10-3×1.0 mol X L
X="1.12" L
答:得到标准状况下氢气的体积1.12 L。
试题分析:本题考察的是化学反应计算,在本题中,铁粉是足量的,因此在计算时不能以铁粉为切入点,而应该以盐酸为切入点来进行计算即可。
点评:本题属于简单计算,抓住利用方程式计算,物质的量之比等于方程式计量数之比,注意有时还需换算单位。

练习册系列答案
相关题目
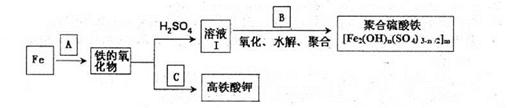


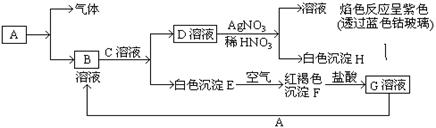

 过滤
过滤 洗涤
洗涤 过滤
过滤