题目内容
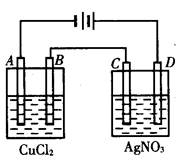
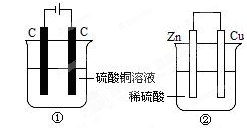
400 mL NaNO3和AgNO3的混合溶液中c(NO3—)=4mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到11.2L气体(标准状况),假设电解后溶液体积仍为400 mL。回答下列问题:
(1)把下列电极方程式补充完整:
阴极: 、2H+ + 2e- = H2
阳极:
(2)上述电解过程中转移电子的物质的量为 。
(3)电解后溶液中的c(H+)为
(1)把下列电极方程式补充完整:
阴极: 、2H+ + 2e- = H2
阳极:
(2)上述电解过程中转移电子的物质的量为 。
(3)电解后溶液中的c(H+)为
(1)阴极 Ag++e-=Ag 。阳极 4OH一—4e一=2H2O+O2↑。
(2) 2mol (3) 2.5mol.L-1
(2) 2mol (3) 2.5mol.L-1
阳极附近有NO和OH-,OH-放电,4OH?-4e-=2H2O+O2↑
阴极附近有Ag+和H+,氧化性Ag+>H+,Ag+先放电,Ag++e-=Ag,2H++2e-=H2↑
生成的V(H2)=V(O2)=11.2L,n=0.5mol;转移电子为0.5mol×4=2mol;c(H+)=2.5mol/L。
阴极附近有Ag+和H+,氧化性Ag+>H+,Ag+先放电,Ag++e-=Ag,2H++2e-=H2↑
生成的V(H2)=V(O2)=11.2L,n=0.5mol;转移电子为0.5mol×4=2mol;c(H+)=2.5mol/L。

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目