题目内容
在容积为2升的密闭容器中,有反应:mA(g)+nB(g) pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为
 pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为| A.3:1:2:2 | B.1:3:2:2 | C.3:1:2:1 | D.1:1:1:1 |
A
若压缩容器的体积,发现A与C的百分含量不变,即该反应为等体积反应,C错;
B的平均反应速度VB=a/15mol·L-1·min-1,即B的浓度变化为a/15mol·L-1·min-1×5 min= a/3mol·L-1
由方程式:mA(g)+nB(g) pC(g)+qD(g),
pC(g)+qD(g),
变化的量:amol·L-1 a/3mol·L-1 2a/3 mol·L-1 x
由于反应为等体积反应,即可得amol·L-1+a/3mol·L-1="=2a/3" mol·L-1 +x;x="=2a/3" mol·L-1;
根据化学反应过程中,变化的量之比=化学计量数之比,可得m:n:p:q=3:1:2:2,所以正确选项为A;
B的平均反应速度VB=a/15mol·L-1·min-1,即B的浓度变化为a/15mol·L-1·min-1×5 min= a/3mol·L-1
由方程式:mA(g)+nB(g)
 pC(g)+qD(g),
pC(g)+qD(g),变化的量:amol·L-1 a/3mol·L-1 2a/3 mol·L-1 x
由于反应为等体积反应,即可得amol·L-1+a/3mol·L-1="=2a/3" mol·L-1 +x;x="=2a/3" mol·L-1;
根据化学反应过程中,变化的量之比=化学计量数之比,可得m:n:p:q=3:1:2:2,所以正确选项为A;

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
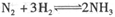 ,在t1时刻达到平衡。保持温度和压强不变,在t2时刻,再通入一部分NH3,反应速率(v)与时间(t)的关系曲线正确的是( )
,在t1时刻达到平衡。保持温度和压强不变,在t2时刻,再通入一部分NH3,反应速率(v)与时间(t)的关系曲线正确的是( )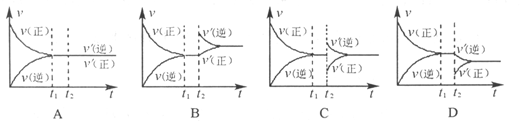
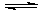 2C(气)+xD(气)+Q经5min达平衡,此时生成2mol C,测得D的平均反应速率为0.1mol·(L·min)-1,下列说法中正确的是
2C(气)+xD(气)+Q经5min达平衡,此时生成2mol C,测得D的平均反应速率为0.1mol·(L·min)-1,下列说法中正确的是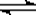 2NH3(g)正反应放热,下列说法错误的是
2NH3(g)正反应放热,下列说法错误的是 NaCl(l)+K(g)(正反应吸热)
NaCl(l)+K(g)(正反应吸热) 。
。
 4 C(g),达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1,且A的质量分数为w%。保持温度不变,再充入A、B、C的物质的量分别为a、b、c,则下列说法正确的是
4 C(g),达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1,且A的质量分数为w%。保持温度不变,再充入A、B、C的物质的量分别为a、b、c,则下列说法正确的是 量分数小于w%
量分数小于w% N2O4,所得混合气体中NO2的体积百分含量为40%,此时,混合气体的平均分子量为
N2O4,所得混合气体中NO2的体积百分含量为40%,此时,混合气体的平均分子量为
 ,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加人CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加人CH3OH,反应到某时刻测得各组分的物质的量浓度如下: