题目内容
金属的防腐常用方法有:
| A.覆盖油脂; | B.覆盖油漆; | C.覆盖塑料; | D.电镀金属; E.电化学保护法; F.制成不锈钢。请为以下钢铁制品选择一种适当的防锈方法(填写序号 ): |
(4)电线 ,(5)铁钳的转动部位 ,(6)自行车的钢圈 。
(1)B (2)F (3)E (4)C (5)A (6)D
解析试题分析:(1)邮筒常刷绿色油漆来防止金属腐蚀。选项为B。(2)手术刀制成不锈钢。也就是减少其中碳元素的含量,加入合金元素导合适的范围。选项为F。(3)海水中的钢闸门采用外加电源的阴极保护法来防止其锈蚀,属于电化学保护法。选项为E。(4)电线为防止漏电及金属腐蚀外面包裹塑料。选项为C。(5)铁钳的转动部位:铁钳在使用时经常会在各种环境中,腐蚀很快,为防止因腐蚀而转动不灵活,常加些煤油或机油、食用油等物质。选项为A。(6)自行车的钢圈:自行车的车轮是钢铁材料,为防止因阴雨天使用引起锈蚀,常进行电镀处理,覆盖一层铬、镍等耐腐蚀的金属。
考点:考查常用金属制品的防腐方法等相关知识。

 小学课时特训系列答案
小学课时特训系列答案实验发现,在FeCl3酸性溶液中加入少量锌粉后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如图所示的原电池装置。下列有关说法中正确的是( )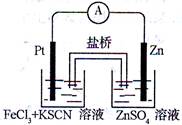
| A.该原电池的正极反应是:Zn-2e— =Zn2+ |
| B.Pt电极表面生成大量气泡 |
| C.左烧杯中溶液的红色逐渐褪去 |
| D.生成的Fe2+通过盐桥可以和锌直接反应生成Fe |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为: Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2+H2O+2e—→Mn2O3+2OH— |
| C.外电路中每通过O.2mol电子,锌的质量理论上减小6.5g[ |
| D.电池工作时,电子由负极通过电解液流向正极 |
298K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+ 立即被还原 成Fe2+。据此某学习小组设计如图所示的原电池装置。下列有关说法正确的是: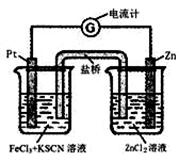
| A.正极反应为Zn-2e-→Zn2+ |
| B.左烧杯中溶液的红色变浅 |
| C.Pt电极上有气泡出现 |
| D.该电池总反应为3Zn+2Fe3+=2Fe+3Zn2+ |
有关金属腐蚀的叙述正确的是
| A.生铁抗腐蚀能力比纯铁强 |
| B.钢瓶在储存液氯前彻底干燥可减缓腐蚀 |
| C.水库铁闸与直流电源正极相连可减缓腐蚀 |
| D.常温下浓硝酸比浓盐酸更易使铁腐蚀 |
下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )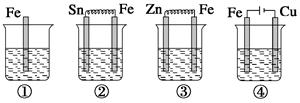
| A.②>①>③>④ | B.④>②>①>③ |
| C.④>②>③>① | D.③>②>④>① |
下图是某同学设计的原电池装置,下列叙述中正确的是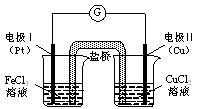
| A.电极Ⅰ上发生还原反应,作原电池的负极 |
| B.电极Ⅱ的电极反应式为:Cu2++2e-=" Cu" |
| C.该原电池的总反应为:2Fe3++Cu= Cu2++2Fe2+ |
| D.盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
下图为摇摆电池(Rocking chair battery)的工作原理图,在充放电过程中,Li+在两极之间“摇来摇去”,其总反应为:LiCoO2+6C Li1-xCoO2+LixC6。下列有关说法正确的是
Li1-xCoO2+LixC6。下列有关说法正确的是
| A.放电时,负极反应LiCoO2 – xe- =Li(1-x)CoO2 + xLi+ |
| B.充电时,A极发生氧化反应 |
| C.充电时,Li+穿过隔离膜向B极移动 |
| D.当B极失去Xmol电子,电池消耗 6 mol C |
 Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是: