��Ŀ����
ij��ϵ�д������·�Ӧ��
��H2S��4H2O��8e �� SO42����10H��
��2IO3����12 H����10e �� I2��6H2O
��1����Ӧ����H2S��__________������Ӧ������___________ ��Ӧ�����������ԭ������
��2�����ڷ�Ӧ����ʧȥ0��2 mol ���ӣ���Ӧ���п����� g I2��
��3��д������ƽ����������ⷴӦ�Ļ�ѧ����ʽ��ͬʱ�������ת�Ƶķ������Ŀ��
_______________________________________________________________________��
��4����������Ӧ����֪ ��
a�������ԣ�K2SO4 �� KIO3 b�����ԣ�HIO3 �� H2SO4
c����ԭ�ԣ�H2S �� I2 d����Ӧ��������Һ����������
��1����ԭ����ԭ ����1�֣���2�֣�
��2��5��08��2�֣�
��3�� ��3�֣�����ʽ2�֣�����ת��1�֣�
��3�֣�����ʽ2�֣�����ת��1�֣�
��4��cd��1�֣�
��������
���������
��1�����ϼ����ߵķ�Ӧ������ԭ������Ԫ�صļ�̬������ۣ���Ϊ��ۣ�������ԭ��Ӧ��
��2���⣺������I2������Ϊx
5H2S�� 40e -�� 8 IO3���� 4 I2
40 4*127*2
0��2 x x= 5��08
��3����*5+��*4 ��5H2S��8KIO3 = 4K2SO4��4I2 ��H2SO4��4H2O
��4����ԭ�ԣ���ԭ������ԭ���� �������ԣ������������������Ϊ��ˮ�����ɣ����Լ�����
���㣺���⿼��������ԭ��Ӧ��֪ʶ��

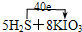 =4K2SO4+4I2+H2SO4+4H2O
=4K2SO4+4I2+H2SO4+4H2O