题目内容
(15分)
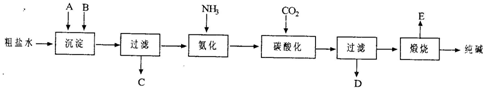
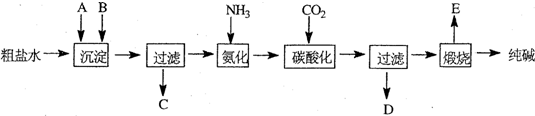
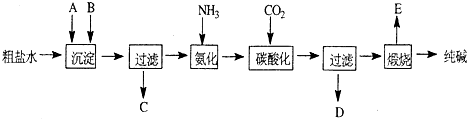
工业生产纯碱的工艺流程示意图如下:

完成下列填空:
(1)沉淀剂A来源于石灰窑厂,写出A、B的化学式。
A B
(2)实验室提纯粗盐的实验操作依次为:取样、 、沉淀、 、 。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象 。碳酸化时没有析出碳酸钠晶体,其原因是 。
(4)碳酸化后过滤,滤液D最主要的成分是 (填写化学式),检验这一成分的阴离子的具体方法: 。
(5)向滤液D中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有 (填a、b、c字母) 。这样做使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 的循环,这就是有名的侯氏制碱法。
a.增大NH4+的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:
(注明你的表达式中所用的有关符号的含义)
(1)Ca(OH)2或CaO;Na2CO3;(2分)
(2)溶解;过滤;蒸发结晶;(3分)
(3)有晶体析出(或出现浑浊);碳酸钠溶解度比碳酸氢钠大;(2分)
(4)NH4Cl;取样,加硝酸酸化,加硝酸银,有白色沉淀,该阴离子是氯离子;(3分)
(5)a;(1分)
析出NH4Cl后的母液重新氨化(1分)
(6)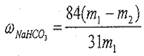 (m1为加热前纯碱的质量,m2为加热后的质量)(2分)
(m1为加热前纯碱的质量,m2为加热后的质量)(2分)
【解析】