��Ŀ����
��13�֣��ҹ��������Ϸ��ֺ�ʹ��ͭ��ͭ������Ĺ���֮һ��ֱ������ͭ���仯�����ڹ�ũҵ��������Ȼ���Ź㷺��Ӧ�á�
��1����ҵ�Ͽ����û�ͭ����Ҫ�ɷ�CuFeS2��Ϊԭ��ұ��ͭ����Ҫ��Ӧ����:
�� 2CuFeS2+4O2=Cu2S+3SO2+2FeO �� 2Cu2S + 3O2=2SO2+2Cu2O�� Cu2S+ 2Cu2O="6Cu+" SO2
�ڢ��б������뱻��ԭԪ��ԭ�ӵ����ʵ���֮��Ϊ ������3mol CuFeS2����3molCu������������O2�����ʵ���Ϊ ��
��2��������Cu2O������ϡ���ᣬ�õ���ɫ��Һ�ͺ�ɫ���壬�������ø����ʼ��鹤ҵ��ұ��ͭ�õ��Ĵ�ͭ���Ƿ���Cu2O��д���˷�Ӧ�����ӷ���ʽ ��
��3����ʴӡˢ��·�ķ�Һ�к��д�����CuCl2��FeCl2��FeCl3�������ŷŽ����»�����Ⱦ����Դ���˷ѣ� Ϊ��ʹFeCl3ѭ�����úͻ���CuCl2������������������̣�
���Լ�Y������ ������X����� ���ѧʽ����
����������1L��Һ�к�CuCl2��FeCl2��FeCl3�����ʵ���Ũ�Ⱦ�Ϊ0.5mol��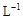 �� �����Cl2��������Xʹ��Һ��pH�� ��Χʱ������Һ������ֲ��䣩����Ԫ����ȫת��ΪFe(OH)3����CuCl2������������( KSP [Fe(OH)3]=1.0��10��38�� KSP[Cu(OH)2]=2.0��10��20 �� lg5=0.7)
�� �����Cl2��������Xʹ��Һ��pH�� ��Χʱ������Һ������ֲ��䣩����Ԫ����ȫת��ΪFe(OH)3����CuCl2������������( KSP [Fe(OH)3]=1.0��10��38�� KSP[Cu(OH)2]=2.0��10��20 �� lg5=0.7)
��13�֣�
��1��1�s6 ��2�֣��� 7.5mol��3�֣�û��λ��1�֣���
��2��Cu2O��2H+��Cu��Cu2+��H2O ��2�֣�û��ƽ��1�֣���ѧʽ��0�֣�
��3����������Ȼ��⣨1�֣���CuO ��2�֣����� 3.0��4.3��3�֣�
���������������1�� Cu2S+ 2Cu2O="6Cu+" SO2�У���������Ԫ�ؼ����ϼ����ߵ�Ԫ����SԪ�أ�����ԭ��Ԫ�ؼ����ϼ۽��͵�Ԫ����CuԪ�أ��ɷ���ʽ��֪�����б������뱻��ԭԪ��ԭ�ӵ����ʵ���֮��Ϊ1:6��
�ɢٵ�6CuFeS2��12O2��3Cu2S�� �ɢڵ� 2Cu2S �� 3O2��2Cu2O�� �ɢ�Cu2S�� 2Cu2O��6Cu���������յù�ϵʽ6CuFeS2��15O2��6Cu������3mol CuFeS2����3molCu������������O2�����ʵ���Ϊ7.5mol��
��2��������Cu2O������ϡ���ᣬ�õ���ɫ��Һ�ͺ�ɫ���壬����������ԭ��Ӧ���ۣ���ɫ��ҺΪ����ͭ��Һ����ɫ����Ϊ����ͭ�����ӷ���ʽΪCu2O��2H+��Cu��Cu2+��H2O��
��3�������������������Ȼ�������Ҫ�Լ�Y��ϡ������Ȼ��⣻����X��Ŀ���ǵ�����ҺpH��ʹ�����ӳ���������Ϊ�˲������µ����ʣ�X���ѡ��CuO��
�ڼ���������ͭ���ӵ�Ũ������0.5mol/L,�����ӵ�Ũ��Ϊ1.0mol/L�����������������ܶȻ���������������ȫ����ʱ��c��OH-��3=1.0��10��38 /1.0��10��5mol��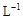 �� ��c��OH-��=1.0��10��11mol��
�� ��c��OH-��=1.0��10��11mol��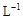 �� pH=3����ͭ���ӿ�ʼ����ʱ��c��OH-��2=2.0��10��20 /0.5=4.0��10��20mol��
�� pH=3����ͭ���ӿ�ʼ����ʱ��c��OH-��2=2.0��10��20 /0.5=4.0��10��20mol��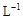 ��c��OH-��=2.0��10��10mol��
��c��OH-��=2.0��10��10mol��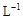 ��pH=4.3��������Ԫ����ȫת��ΪFe(OH)3����CuCl2����������ʱ��Һ��pH�ķ�Χ��3.0��4.3��
��pH=4.3��������Ԫ����ȫת��ΪFe(OH)3����CuCl2����������ʱ��Һ��pH�ķ�Χ��3.0��4.3��
���㣺����������ԭ��Ӧ�ļ��㣬�Լ���ѡ����ҺpH�ļ���

 ��ս100��Ԫ����Ծ�ϵ�д�
��ս100��Ԫ����Ծ�ϵ�д�Ϊ�˷�ֹǹ֧���⣬����ǹ֧�ĸ����������NaNO2��NaOH�Ļ��Һ�н��л�ѧ����ʹ���������������Fe3O4�����ܵı����㡪����������������̿������л�ѧ����ʽ��ʾ��
��3Fe NaNO2
NaNO2 5NaOH �� 3Na2FeO2
5NaOH �� 3Na2FeO2 H2O
H2O NH3��
NH3��
�� Na2FeO2 NaNO2
NaNO2 H2O �� Na2Fe2O4
H2O �� Na2Fe2O4 NH3��
NH3�� NaOH
NaOH
��Na2FeO2 Na2Fe2O4
Na2Fe2O4 2H2O
2H2O Fe3O4
Fe3O4 4NaOH
4NaOH
��1����ƽ��ѧ����ʽ�ڡ�
��2��������Ӧ���л�ԭ��Ϊ ������ԭ���� ������1mol Na2FeO2���ɣ���Ӧ���� mol����ת�ơ�
��3�������γɡ��������Ĺ��̣�����˵����ȷ���ǡ��������������������������������� ��
| A�����������̲��������Ⱦ | B����Ӧ�����ɵ��������������п���ʴ���� |
| C����Ӧ�٢ڢ۾���������ԭ��Ӧ | D����Ӧ�٢��е���������ΪNaNO2 |
ij��ѧ��ȤС����̽��±�ص��ʵ������Ե�ʵ���з��֣����������Ȼ�������Һ�У�����1��2����ˮ������Һ�ʻ�ɫ��ԭ����ʲô��Br2�ܷ�����Fe2����Fe3����Br2˭�������Ը�ǿ��
(1)��ͬѧ��Ϊ��Br2��������Fe2����Fe3���������Դ���Br2���������������ԭ���ǻ�ѧ��Ӧ���£���Һ�ʻ�ɫ�Ǻ� (�ѧʽ����ͬ)���¡�
(2)��ͬѧ��Ϊ��Br2��Fe2������ΪFe3����Fe3����������С��Br2���������������ԭ���ǻ�ѧ��Ӧ���£�����Һ�ʻ�ɫ�Ǻ� ���¡�
(3)��ͬѧΪ��֤��ͬѧ�Ĺ۵㣬ѡ�������Լ�����Ƴ����ַ�������ʵ�飬��ͨ���۲�ʵ������֤������ͬѧ�Ĺ۵�����ȷ�ģ���ѡ�õ��Լ���a.��̪�Լ���b.CCl4��c.��ˮ�ƾ���d.KSCN��Һ���������±���д����ͬѧѡ�õ��Լ���ʵ���й۲쵽������(�Լ������)
| ѡ���Լ� | ʵ������ |
| ����1 | |
| ����2 | |
(4)�����ԣ�Br2��Fe3��������FeCl2�е���1��2����ˮ����Һ�ʻ�ɫ��������Ӧ�����ӷ���ʽ�� ��
(5)��������ʵ���Ʋ⣬����ϡ�廯������Һ��ͨ�����������ȱ������������� ����100 mL FeBr2��Һ��ͨ��2.24 L Cl2(��״��)����Һ����
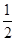 ��Br���������ɵ���Br2����ԭFeBr2��Һ�����ʵ���Ũ���� ��
��Br���������ɵ���Br2����ԭFeBr2��Һ�����ʵ���Ũ���� �� �۲����о��������ʵ�һ�ֻ���������һͬѧ��һС�������¶���ڿ����У��۲쵽������������ɫ���ٱ�Ұ����ڱ��ɫ���۳���Һ�Ρ��ܰ�ɫ���壬����˵������ȷ���� ( )
| A���ٷ�����������ԭ��Ӧ | B���ڱ��ɫ����Ϊ������̼���� |
| C������̼�������տ����е�ˮ�����γ�����Һ | D����ֻ���������仯 |

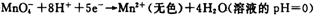
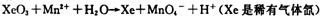



 2Fe(s)��3CO(g) ��H����492.7kJ/mol
2Fe(s)��3CO(g) ��H����492.7kJ/mol