题目内容
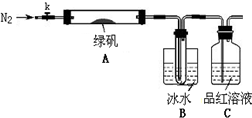
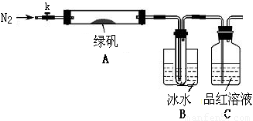
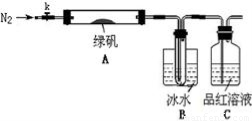
某校的化学兴趣小组利用下列实验装置探究二氧化硫的性质,已知Na2SO3+H2SO4
(1)实验室检验二氧化硫所用的试剂是________________。
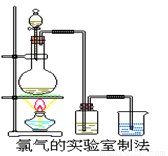
(2)E是贮存有某种气体的针管,该气体能使湿润的红色石蕊试纸变蓝,写出实验室制备这种气体的化学方程式:________________________________。
(3)装置D的作用是________________,反应的离子方程式是________________。
(4)A中的反应结束后,关闭活塞K1,打开活塞K2,将贮存在E中的气体注入B中,观察到B中的现象是________________,反应的离子方程式是________________。
(5)反应结束后,取少量的C中溶液,加入氯化钡溶液,观察到有白色沉淀生成,请你写出氯水与二氧化硫反应的化学方程式:________________________________。
(1)品红溶液
(2)2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O(合理答案均可)
CaCl2+2NH3↑+2H2O(合理答案均可)
(3)吸收多余的二氧化硫,防止污染环境 2OH-+SO2![]()
![]() +H2O
+H2O
(4)白色沉淀 Ba2++2NH3+H2O+SO2![]() BaSO3↓+2
BaSO3↓+2![]()
(5)Cl2+2H2O+SO2![]() H2SO4+2HCl
H2SO4+2HCl
解析:(1)SO2有使品红溶液褪色的特点.(2)E为碱性气体,高中阶段只学过NH3.(3)SO2有毒,所以必须进行尾气处理.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目