题目内容
(8分)A、B、C、D、E五种短周期元素,原子序数依次增大。A与B、C分别构成电子数相等的化合物W、K,且W是一种能产生温室效应的气体;D元素最外层电子数是次外层电子数的3倍。A、D、E构成化合物Y,A、B、C、D构成化合物X,且X、Y均为阳离子和阴离子个数比是1∶1的离子化合物。
回答下列问题:
(1)Y的电子式为________;W形成________晶体。
(2)与E同主族且为第7周期的元素原子序数为________。
(3)在同主族氢化物的递变性质中,K的沸点反常,这可以用________来解释(填字母序号)。
A.共价键 B.离子键
C.氢键 D.范德华力
回答下列问题:
(1)Y的电子式为________;W形成________晶体。
(2)与E同主族且为第7周期的元素原子序数为________。
(3)在同主族氢化物的递变性质中,K的沸点反常,这可以用________来解释(填字母序号)。
A.共价键 B.离子键
C.氢键 D.范德华力

此题为元素推断题。D元素最外层电子数是次外层电子数的3倍,故其次外层为第一层,该元素的原子序数为8,即O元素;由于A、B、C、D、E五种短周期元素,原子序数依次增大。A与B、C分别构成电子数相等的化合物W、K,且W是一种能产生温室效应的气体,常见的温室气体有CH4、CO2、O3等,根据B的原子序数小于O元素,故其只能是C元素,则A是H元素,C是N元素;由于A、D、E构成化合物Y,A、B、C、D构成化合物X,且X、Y均为阳离子和阴离子个数比是1∶1的离子化合物,故Y是NaOH,X是NaHCO3;据此可回答(1)氢氧化钠的电子式为: ;甲烷形成的晶体为分子晶体;(2)根据周期表的结构,其前六周期含有的元素总数为86,故与E同主族且为第7周期的元素原子序数为87;(3)氨气的沸点反常的原因是其结构中含有氢键。
;甲烷形成的晶体为分子晶体;(2)根据周期表的结构,其前六周期含有的元素总数为86,故与E同主族且为第7周期的元素原子序数为87;(3)氨气的沸点反常的原因是其结构中含有氢键。
 ;甲烷形成的晶体为分子晶体;(2)根据周期表的结构,其前六周期含有的元素总数为86,故与E同主族且为第7周期的元素原子序数为87;(3)氨气的沸点反常的原因是其结构中含有氢键。
;甲烷形成的晶体为分子晶体;(2)根据周期表的结构,其前六周期含有的元素总数为86,故与E同主族且为第7周期的元素原子序数为87;(3)氨气的沸点反常的原因是其结构中含有氢键。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
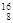 O 与
O 与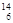 C互为同位素
C互为同位素 Ce、
Ce、 Ce、
Ce、 Ce、
Ce、 Ce,它们互为同位素
Ce,它们互为同位素
 键的键数之比为 ,其化学性质 (填“活泼”或“稳定”):
键的键数之比为 ,其化学性质 (填“活泼”或“稳定”):