题目内容
X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有如图1-3-29所示的转化关系(部分反应物、产物及反应条件已略去)。
图1-3-29
请回答:
(1)W的电子式是___________________________________。
(2)X与Y在溶液中反应的离子方程式是__________________________________________。
(3)X含有四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用图1-3-30装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
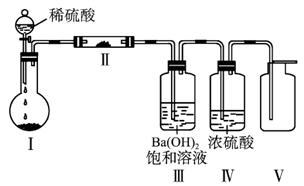
图1-3-30
①装置Ⅰ中反应的化学方程式是 __________________________________________,装置Ⅱ中物质的化学式是___________________________________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是______________,所需仪器装置是_______ (从上图选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是______________________________________________________。
解析:由题意知X、Y、Z均含有,钠元素,又由X![]() Z知X不稳定,受热易分解,可能为弱酸酸式盐;又由于Z
Z知X不稳定,受热易分解,可能为弱酸酸式盐;又由于Z![]() W(无色无味气体)则W应为CO2,Z为Na2CO3,X为NaHCO3;由NaHCO3+Y
W(无色无味气体)则W应为CO2,Z为Na2CO3,X为NaHCO3;由NaHCO3+Y![]() Na2CO3,则Y一定为NaOH,则(1)—(2)易于解决。(3)由于装置Ⅲ中产生白色沉淀,则产生气体中必含CO2,气体通过浓H2SO4后,收集 到无色气体,则必为氧气,则说明装置Ⅱ中必为Na2O2,则(Ⅰ)中物质可能为Na2CO3或NaHCO3。若由两种元素组成的物质,经催化作用得到O2,则该化合物为H2O2,所用装置为Ⅰ、Ⅳ、Ⅴ。(4)若向Na2CO3溶液中通入Cl2,则产生的漂白性物质为NaCl,同时生成NaHCO3,则必定还有NaClO生成,所以该反应的化学方程式为2Na2CO3+Cl2+H2O====NaClO+NaCl+2NaHCO3。
Na2CO3,则Y一定为NaOH,则(1)—(2)易于解决。(3)由于装置Ⅲ中产生白色沉淀,则产生气体中必含CO2,气体通过浓H2SO4后,收集 到无色气体,则必为氧气,则说明装置Ⅱ中必为Na2O2,则(Ⅰ)中物质可能为Na2CO3或NaHCO3。若由两种元素组成的物质,经催化作用得到O2,则该化合物为H2O2,所用装置为Ⅰ、Ⅳ、Ⅴ。(4)若向Na2CO3溶液中通入Cl2,则产生的漂白性物质为NaCl,同时生成NaHCO3,则必定还有NaClO生成,所以该反应的化学方程式为2Na2CO3+Cl2+H2O====NaClO+NaCl+2NaHCO3。
答案:(1)![]()
(2)![]() + OH-====
+ OH-====![]() +H2O
+H2O
(3)①Na2CO3+H2SO4====Na2SO4+CO2↑+H2O
或2NaHCO3+H2SO4====Na2SO4+2CO2↑+2H2O Na2O2
②H2O2 Ⅰ、Ⅳ、Ⅴ
(4)2Na2CO3+Cl2+H2O====NaClO+NaCl+2NaHCO3

 (2011?江苏)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.
(2011?江苏)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.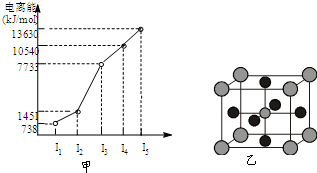 有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.
有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.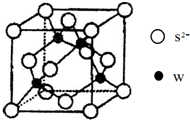 原子序数小于36的X、Y、Z、W四种元素,其中X原子基态时2p原子轨道上有3个未成对电子,Y原子基态时最外层电子数是其内层电子数的3倍,Z元素的最高价氧化物的水化物的酸性最强,W的原子序数为30.
原子序数小于36的X、Y、Z、W四种元素,其中X原子基态时2p原子轨道上有3个未成对电子,Y原子基态时最外层电子数是其内层电子数的3倍,Z元素的最高价氧化物的水化物的酸性最强,W的原子序数为30.