题目内容
10.下列物质的熔、沸点高低顺序正确的是( )| A. | 金刚石,晶体硅,碳化硅 | B. | CI4>CBr4>CCl4>CH4 | ||
| C. | MgO>CsCl>NaCl | D. | Na>Mg>Al |
分析 A.原子晶体中,熔沸点高低与键长成反比;
B.分子晶体中,熔沸点与相对分子质量成正比;
C.离子晶体中,熔沸点与电荷成正比、与离子半径成反比;
D.金属晶体中,熔沸点与半径成正比.
解答 解:A.原子晶体中,熔沸点高低与键长成反比,这几种物质都是原子晶体,键长C-C<C-Si<Si-Si,所以熔沸点金刚石>碳化硅>晶体硅,故A错误;
B.分子晶体中,熔沸点与相对分子质量成正比,相对分子质量CI4>CBr4>CCl4>CH4,所以熔沸点CI4>CBr4>CCl4>CH4,故B正确;
C.离子晶体中,熔沸点与电荷成正比、与离子半径成反比,镁离子和氧离子都两个单位电荷,钠离子、铯离子和氯离子都带一个单位电荷,且铯离子半径大于钠离子,所以熔沸点MgO>NaCl>CsCl,故C错误;
D.金属晶体中,熔沸点与半径成正比,半径Na>Mg>Al,所以熔沸点Al>Mg>Na,故D错误;
故选B.
点评 本题考查离子晶体、原子晶体、金属晶体、分子晶体熔沸点高低判断,侧重考查知识运用,明确晶体类型及晶体熔沸点高低影响因素即可解答,题目难度不大.

练习册系列答案
相关题目
20.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑.
(2)实验①的目的是研究温度对H2O2分解速率的影响,实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中 | 试管A中不再产生气泡 试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液 | 试管A、B中均未见气泡产生 |
(2)实验①的目的是研究温度对H2O2分解速率的影响,实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
1.下列物质的说法错误的是( )
| A. | 某实验过程中得到一定量的碘水,可用裂化汽油从碘水中萃取出碘 | |
| B. | 芳香烃主要来自于煤焦油和石油化工中的催化重整 | |
| C. | 常压分馏得到的汽油是混合物,没有固定的沸点 | |
| D. | 乙烯是轻质油裂解的产物,其产量可用来衡量一个国家的石油化工发展水平 |
5.将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中,然后向小烧杯中加入盐酸,反应剧烈醋酸逐渐凝固.下列说法正确的是( )
| A. | NH4HCO3与盐酸的反应是放热反应 | |
| B. | 该反应中,热能转化为产物内部的能量 | |
| C. | 反应物的总能量高于生成物的总能 | |
| D. | 该反应的反应物和生成物的能量高低与醋酸的凝固无关 |
15.下列关于铷的叙述中正确的是( )
| A. | 硝酸铷是离子化合物 | |
| B. | 在钠、钾、铷三种单质中,铷的熔点最高 | |
| C. | 氢氧化铷是弱碱 | |
| D. | 它位于周期表的第四周期、第ⅠA族 |
20.下列关于铷(Rb)的叙述正确的是( )
| A. | 它位于周期表的第五周期,第I A族 | |
| B. | 氢氧化铷是弱碱 | |
| C. | 在钠、钾、铷3种单质中,铷的熔点最高 | |
| D. | 硝酸铷是离子化合物 |
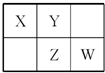 四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.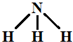 (写结构式);
(写结构式); ;
;