题目内容
12.元素的原子结构决定其性质和在周期表中的位置.下列说法正确的是( )| A. | 元素原子的最外层电子数等于元素的最高化合价 | |
| B. | 多电子原子中,在离核较近的区域内运动的电子能量较低 | |
| C. | 若M+和R2-的核外电子层结构相同,则原子序数:R>M | |
| D. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
分析 A.氧元素、氟元素没有最高正化合价,过渡元素最高正化合价一般大于最外层电子数;
B.电子能量越低,挣脱原子核束缚的能力弱,在距离原子核近的区域运动;
C.若M+和R2-的核外电子层结构相同,则核外电子数相同,阳离子核外电子数=质子数-所带电荷数,阳离子核外电子数=质子数+所带电荷数;
D.过渡元素包括副族与Ⅷ族元素.
解答 解:A.氧元素、氟元素没有最高正化合价,氧、氟元素除外,其它主族元素最高正化合价等于其最外层电子数,过渡元素最高正化合价一般大于最外层电子数,故A错误;
B.电子能量高,挣脱原子核束缚的能力强,在距离原子核远的区域运动,电子能量越低,挣脱原子核束缚的能力弱,在距离原子核近的区域运动,故B正确;
C.若M+和R2-的核外电子层结构相同,则核外电子数相同,阳离子核外电子数=质子数-所带电荷数,阳离子核外电子数=质子数+所带电荷数,则原子序数:M>R,故C错误;
D.过渡元素包括副族与Ⅷ族元素,故D错误,
故选B.
点评 本题考查元素周期表与元素周期律、核外电子排布等,比较基础,注意对基础知识的掌握,注意一些元素的特殊性.

练习册系列答案
相关题目
2.下列基态原子或离子的电子排布式错误的是( )
| A. | K 1s22s22p63s23p64s1 | B. | Mg2+ 1s22s22p6 | ||
| C. | F- 1s22s22p5 | D. | Br 1s22s22p63s23p63d104s24p5 |
3.如图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )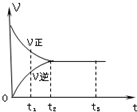

| A. | t1时,只有正反应继续进行 | B. | t2时,反应停止 | ||
| C. | t2-t3,反应不再是可逆反应 | D. | t2-t3,各物质的浓度不再发生变化 |
20.下列粒子中,与K+含有相同电子数的是( )
| A. | F- | B. | Cl- | C. | Br- | D. | I- |
7.下列措施中,能减慢化学反应速率的是( )
| A. | 将块状固体药品研细后再反应 | |
| B. | 将H2O2溶液存放在低温冷暗处 | |
| C. | 用FeCl3溶液作H2O2分解反应的催化剂 | |
| D. | 用2 mol/L H2SO4溶液代替1 mol/L H2SO4溶液与锌粒反应 |
17.利用原电池原理可以探究金属的活动性.
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片做负极(填“正”或“负”),锌片上发生的电极反应式是Zn-2e-=Zn2+;银片上发生的电极反应式是2H++2e-=H2↑.
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g.此时产生标准状况下氢气的体积为4.48L,通过导线的电子的物质的量为0.4mol.
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案.其中能证明铁的金属活动性比铜强的方案是①③④.(填序号)
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片做负极(填“正”或“负”),锌片上发生的电极反应式是Zn-2e-=Zn2+;银片上发生的电极反应式是2H++2e-=H2↑.
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g.此时产生标准状况下氢气的体积为4.48L,通过导线的电子的物质的量为0.4mol.
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案.其中能证明铁的金属活动性比铜强的方案是①③④.(填序号)
| 方 案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| ④将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
4.能在溶液中大量共存的一组离子是( )
| A. | NH4+、Ag+、CO32-、Cl- | B. | Fe3+、H+、I-、HCO3- | ||
| C. | K+、Na+、NO3-、Cl- | D. | H+、Fe2+、SO42-、NO3- |