题目内容
下列各组分子中,都属于含极性键的非极性分子的是( )
分析:不同非金属元素之间形成的共价键为极性键,分子结构对称,正负电荷重心重叠,形成的为非极性分子,以此解答.
解答:解:A.C-H、C-Cl之间都为极性键,结构都为正四面体,为非极性分子,故A正确;
B.CO2为非极性分子,H2S为极性分子,故B错误;
C.H2O为极性分子,故C错误;
D.NH3为三角锥形,为极性分子,HCl为极性分子,故D错误.
故选A.
B.CO2为非极性分子,H2S为极性分子,故B错误;
C.H2O为极性分子,故C错误;
D.NH3为三角锥形,为极性分子,HCl为极性分子,故D错误.
故选A.
点评:本题考查共价键和分子极性的判断,注意把握共价键的形成和分类,把握分子极性的判断,难度不大,注意相关基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

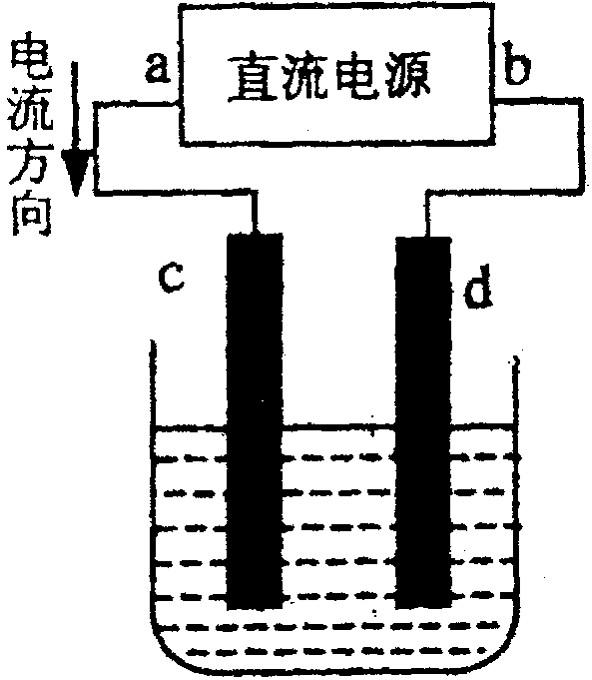
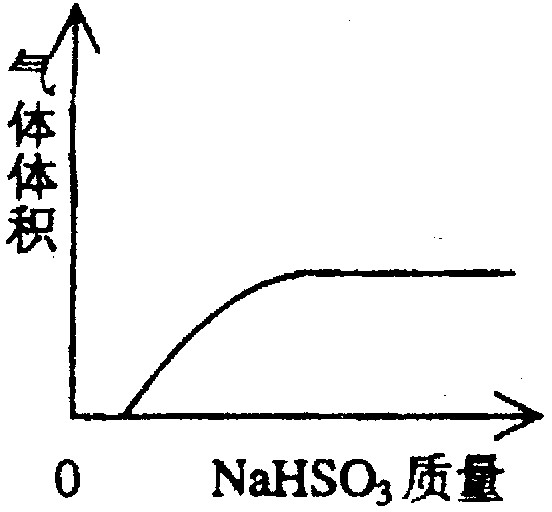
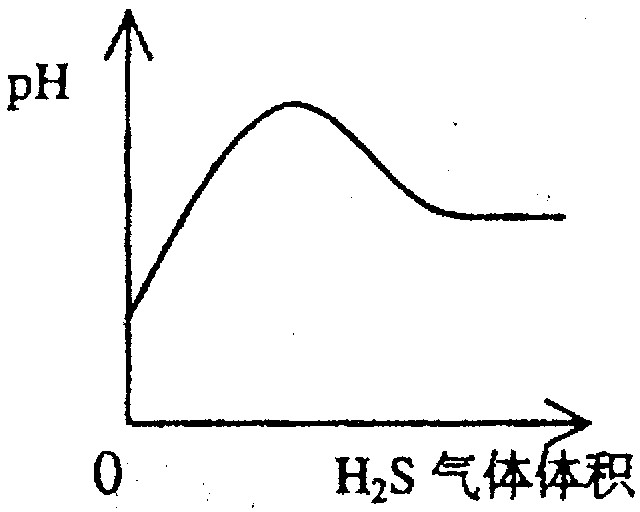
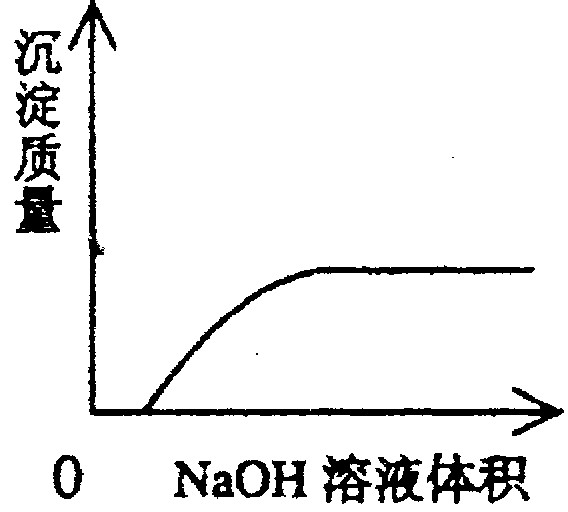

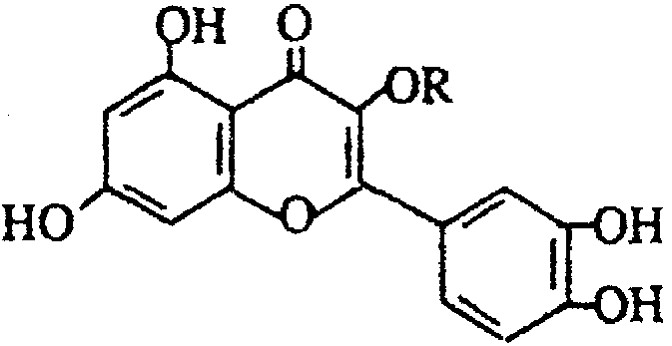
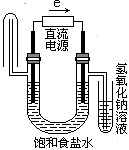 B、
B、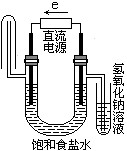
 D、
D、