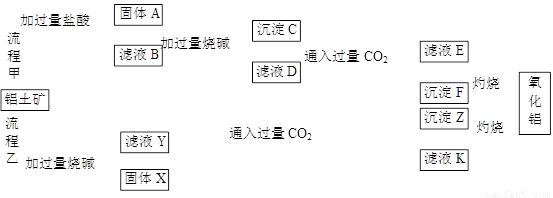��Ŀ����
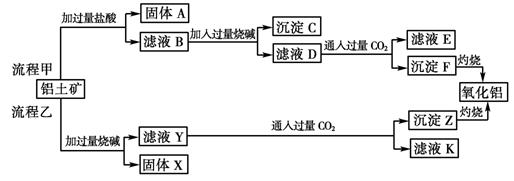
��10�֣���������(��Ҫ�ɷ���Al2O3����SiO2��Fe2O3��MgO������)����ȡ�����������ֹ����������£�

��ش��������⣺
��1�����̼�ͨ�����CO2�����ɳ���F�����ӷ�Ӧ����ʽΪ______________________________________��
(2�����Ҽ����ռ��ܽ�SiO2�Ļ�ѧ��Ӧ����ʽ____________________��
(3)��֤��ҺB��Fe3������ȡ������Һ������________(���Լ�����)��
(4)��ҺE��K�����ʵ���Ҫ�ɷ���________(�ѧʽ)��д�������ʵ�һ����;____________________��
(5)��֪298 Kʱ��Mg(OH)2���ܶȻ�����Ksp��5.6��10��12��ȡ��������ҺB������һ�������ռ����ﵽ�����ܽ�ƽ�⣬���pH��12������¶��²�������Һ�е�c(Mg2��)��________________��
(1) [Al(OH)4]- ��CO2 = Al(OH)3����HCO3����2�֣�
(2) SiO2��2NaOH===Na2SiO3��H2O��2�֣�
(3)���軯��(��������ء�������Һ�Ⱥ�����) ��2�֣�
(4)NaHCO3��1�֣� �ƴ���(�������ͷ۵Ⱥ�����)��1�֣� (5)5.6��10��8 mol/L��2�֣�
����������1����������������������������Ӧ������A�Ƕ������衣B�к����Ȼ������Ȼ������Ȼ�þ���������ᡣ����������ռ����������������������þ��������C������������������þ����D��ƫ�������Լ��������������ƣ�����ͨ��CO2���ɳ���F�ķ���ʽΪ[Al(OH)4]- ��CO2 = Al(OH)3����HCO3����
��2����������ռӦʱ��������������þ����Ӧ������Xʱ������������þ��Y��ƫ�����ơ������ƺ������ռ��˶���������ռӦ�ķ���ʽΪSiO2��2NaOH===Na2SiO3��H2O��
��3�����������ӵ��Լ���KSCN��Һ�ӡ�
��4����ҺD��Y����CO2��Ӧ�����Һ����Ҫ���е�������̼�����ơ�̼�����Ƴ������ƴ���(�������ͷ۵�)��
��5��pH��12������Һ��OH��Ũ����0.01mol��L��1�������ܶȻ������ı���ʽ ��֪����Һ��c(Mg2��)��5.6��10��12/0.0001��5.6��10��8 mol/L��
��֪����Һ��c(Mg2��)��5.6��10��12/0.0001��5.6��10��8 mol/L��

 �������ϵ�д�
�������ϵ�д�