题目内容
某银币(铜、银合金)质量为25g,为测定其元素的质量分数,向其中加入75 mL 12 mol·L-1的浓硝酸使其完全溶解。实验结束后,A中烧瓶内溶液中H+的浓度为2 mol·L-1(反应中HNO3既无挥发也无分解),溶液体积仍为75 mL。
①计算参加反应的硝酸的物质的量是_______ mol。
②写出你设计的测定该银币中银的质量分数的最简单的实验方案(操作步骤及计算式)__________
①计算参加反应的硝酸的物质的量是_______ mol。
②写出你设计的测定该银币中银的质量分数的最简单的实验方案(操作步骤及计算式)__________
①0.75 mol ( 2分)
②将A中溶液倒入烧杯中,然后加入过量的NaCl溶液,过滤、洗涤、烘干、称量,测定AgCl的质量算出银的质量分数(108W÷143.5)/25×100%( 2分)
②将A中溶液倒入烧杯中,然后加入过量的NaCl溶液,过滤、洗涤、烘干、称量,测定AgCl的质量算出银的质量分数(108W÷143.5)/25×100%( 2分)
(1)参加反应的硝酸的物质的量:0.075×12-0.075×2=0.75 mol
(2)合金被硝酸溶解后,银以离子的形式存在,为测定银的质量分数可:将A中溶液倒入烧杯中,然后加入过量的NaCl溶液,过滤、洗涤、烘干、称量,测定AgCl的质量;
设所得AgCl的质量为w克,则银的质量分数为: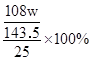
(2)合金被硝酸溶解后,银以离子的形式存在,为测定银的质量分数可:将A中溶液倒入烧杯中,然后加入过量的NaCl溶液,过滤、洗涤、烘干、称量,测定AgCl的质量;
设所得AgCl的质量为w克,则银的质量分数为:
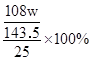

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 2HCl+O2反应中,每生成32g氧气,则转移2NA个电子
2HCl+O2反应中,每生成32g氧气,则转移2NA个电子