题目内容
为了说明稀硝酸与铜反应产生无色的一氧化氮气体,某同学设计了如图8-5所示的实验装置。实验时,将分液漏斗的活塞打开,从U形管的长管口注入稀硝酸,一直到U形管的短管口单孔塞下沿且液面上不再留有气泡为止。关闭活塞,并用酒精灯在U形管短管下微热。当铜丝上有气泡产生时,立即撤去酒精灯。试完成下列问题:
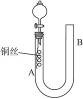
图8-5
(1)反应一段时间后,出现的现象是_____________________________________________。
(2)若将活塞缓缓打开,分液漏斗内的现象是_____________________________________。
(3)写出生成一氧化氮的离子方程式_____________________________________________。
(1)铜丝周围冒气泡,溶液逐渐变蓝,A处液面下降,B处液面上升
(2)产生红棕色气体
(3)3Cu+2![]() +8H+====3Cu2++2NO↑+4H2O
+8H+====3Cu2++2NO↑+4H2O
解析:
装置A处铜与硝酸发生反应:3Cu+2![]() +8H+====3Cu2++2NO↑+4H2O,其现象是铜丝周围产生气泡,铜丝逐渐溶解,溶液变黑,澄清后变为蓝色,因有无色气体产生,压强增大,A处液面下降,B处液面上升。若将分液漏斗活塞打开,A处液面上升,将NO无色气体压入分液漏斗中,与空气接触,产生红棕色气体。
+8H+====3Cu2++2NO↑+4H2O,其现象是铜丝周围产生气泡,铜丝逐渐溶解,溶液变黑,澄清后变为蓝色,因有无色气体产生,压强增大,A处液面下降,B处液面上升。若将分液漏斗活塞打开,A处液面上升,将NO无色气体压入分液漏斗中,与空气接触,产生红棕色气体。

练习册系列答案
相关题目
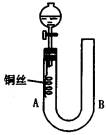
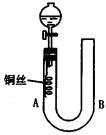
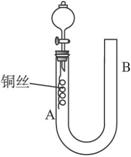
 在U形管短管下微热。当铜丝上有气泡产生时,立即撤去酒精灯。试回答
在U形管短管下微热。当铜丝上有气泡产生时,立即撤去酒精灯。试回答