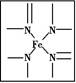
题目内容
A、B、C、D、E是5种短周期元素,原子序数逐渐增大,A的最简单气态氢化物是一种温室气体,A与C、B与C组成的化合物是机动车排出的大气污染物,C和D能形成原子个数比为1∶1和1∶2的两种化合物,E的最高价氧化物的水化物分别与B、D的最高价氧化物的水化物反应生成盐M和N。试回答下列问题:
(1)A在元素周期表中的位置是___,D2C2中含有的化学键有____________。
(2)工业合成B的气态氢化物BH3是放热反应。下列措施中,既能加快反应速率,又能提高原料转化率的是________(填字母序号)。实验室里检验BH3的方法是_________________。
a.升高温度 b.加入催化剂
c.将BH3及时分离出去 d.增大反应体系的压强
(3)盐M和盐N不能同时存在于水溶液中,用离子方程式表示其原因:__。
(4)A的最高价氧化物与D的最高价氧化物的水化物反应生成的正盐溶液呈________性,其原因是___________________(用离子方程式表示)。
(5)已知:A(s)+C2(g)=AC2(g) ΔH=-393.5 kJ·mol-1
AC(g)+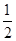 C2(g)=AC2(g) ΔH=-283.0 kJ·mol-1
C2(g)=AC2(g) ΔH=-283.0 kJ·mol-1
则A与C反应生成AC的热化学方程式为____________________________。
(1)第二周期ⅣA族 离子键、共价键
(2)d 用蘸有浓盐酸的玻璃棒靠近导管口,若产生白烟,说明产生的气体为氨气(或用润湿的红色石蕊试纸靠近导管口,若试纸变蓝,说明产生的气体为氨气)
(3)Al3++3AlO2+6H2O=4Al(OH)3↓
(4)碱 CO32-+H2O HCO3-+OH-
HCO3-+OH-
(5)C(s)+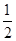 O2(g)
O2(g) CO(g) ΔH=-110.5 kJ·mol-1
CO(g) ΔH=-110.5 kJ·mol-1
解析

三种短周期元素X、Y、Z,它们的原子序数之和为16,X、Y、Z三种元素的常见单质在常温下都是无色气体。已知X原子的最外层电子数是内层电子数的3倍,X和Y的单质直接化合形成气体A,X和Z的单质直接化合形成液态化合物B,Y和Z的单质直接化合形成的化合物C是一种无色有刺激性气味的气体。
请回答下列问题:
(1)Y元素在周期表中的位置是 。
(2)C可在X的单质中燃烧得到Y的单质和化合物B,利用此反应可制成新型的化学电源(KOH溶液做电解质溶液),两个电极均由多孔碳制成,通人的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质是 (填物质名称);负极的电极反应式为 。
(3)C与X的单质反应生成A的化学方程式为 。
(4)常温下,C的水溶液的pH=12,则该溶液中由水电离的C(OH-)= 。若向C溶液中加入等体积、等物质的量浓度的盐酸,所得溶液中水的电离程度 (填“大于”、“等于”或“小于”)相同条件下C溶液中水的电离程度。
(5)在2L密闭容器中放入1molC气体,在一定温度进行如下反应:
2C(g) 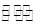 Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
该反应的化学平衡常数表达式是 (用具体物质的化学式表示);平衡时C的转化率为 。
(6)已知:①Y2(g)+2X2(g)=2YX2(g)
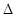 H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。②Y2Z4(g)+X2(g)=Y2(g)+2Z2X(g)
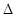 H="-534" kJ·mol-1。
H="-534" kJ·mol-1。则2Y2Z4(g)+2YX2(g)=3Y2(g)+4Z2X(g)
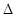 H= kJ·mol-1
H= kJ·mol-1 已知A、B、C、D、E、F六种短周期元素中,A、B、C、D是组成蛋白质的基本元素;A与B的原子序数之和等于C原子核内的质子数;A与E、D与F分别位于同一主族,且F原子核内的质子数是D原子核外电子数的2倍。据此,请回答:
(1)F在周期表中的位置是____________________________。
(2)由A、C、D、F按8:2:4:1原子个数比组成的化合物甲中含有的化学键类型为____________;甲溶液中各离子浓度由大到小的顺序为________________(用离子浓度符号表示)。
(3)化合物乙由A、C组成且相对分子质量为32;化合物丙由A、D组成且分子内电子总数与乙分子内电子总数相等;乙与丙的反应可用于火箭发射(反应产物不污染大气),则该反应的化学方程式为_________________________________________。
(4)由A、D、E、F组成的化合物丁能与硫酸反应并放出刺激性气味的气体,则丁的化学式为________;实验测得丁溶液显弱酸性,由此你能得出的结论是___________________。
(5)由B、A按1:4原子个数比组成的化合物戊与D的常见气态单质及NaOH溶液构成原电池
|
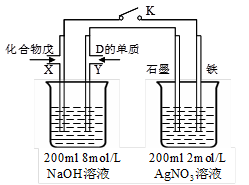
①闭合K,写出左池X电极的反应式__________________________________;
②闭合K,当X电极消耗1.6g化合物戊时(假设过程中无任何损失),则右池两极共放出气体在标准状况下的体积为_________升。
短周期元素X、Y、Z、L、M、Q的原子半径和主要化合价见下表
| 元素代号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
就以上6种元素,用化学用语回答下列问题
(1)同主族的元素是 ,
(2)写出同周期元素间形成的常温下是有毒气体化合物的分子式为 ,
(3)写出不同周期的元素间形成的常温下为液体且难溶于水的任意一种化合物的电子式 。
(4)等质量的X、Y的单质与足量盐酸反应,生成H2的物质的量之比为
(5)写出由表中元素形成的物质间发生常见的置换反应的化学方程式
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
(1)W位于元素周期表第________周期第________族;W的原子半径比X的________(填“大”或“小”)。
(2)Z的第一电离能比W的________(填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是________;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称________。
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的现象是________;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是_________________________________________________。
现有部分前36号元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
| S | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| T | 基态原子3d轨道上有1个电子 |
| X | 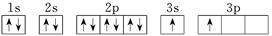 |
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是____________________________________。
R原子的结构示意图是 。
(2)S元素的最常见化合价为________,原因是________________________________________。
(3)T元素原子的价电子构型为________。
(4)X的电子排布图违背了____________。用X单质、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:_________________________________。