题目内容
将固体草酸锰MnC2O4-2H2O放在一个可以称出质量的容器里加热.固体质量随温度的变化的关系如图所示,试通过对该图象数据分析和计算,回答在不同温度范围固体质量变化的原因.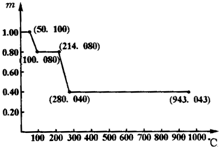

FeC2O4?2H2O→FeC2O4+2H2O
180 144
1.000g x
解得x=0.800g,
则214℃时,结晶水已全部失去,
即在100~214℃时,FeC2O4不分解,结晶水合物失去结晶水;
214℃时,由固体质量在减小,则草酸亚铁分解生成的是氧化亚铁和一氧化碳、二氧化碳,
FeC2O4
FeO+CO2↑+CO↑
144 72
0.8g y
解得y=0.4g,
则214℃~280℃发生草酸亚铁分解分解反应,280℃分解完全;
218℃~943℃内由图象可知,固体质量增加,发生的反应是氧化亚铁被氧化为氧化铁,
4FeO+O2═2Fe2O3
288 320
0.4g z
解得z=0.43,
即218℃~943℃内发生化合反应,
答:加热到50℃不发生反应,加热到100℃~214℃时发生失去结晶水的反应使质量减小,214℃~280℃发生分解反应使固体质量减小,280℃~943℃发生化合反应使固体质量增加.
180 144
1.000g x
解得x=0.800g,
则214℃时,结晶水已全部失去,
即在100~214℃时,FeC2O4不分解,结晶水合物失去结晶水;
214℃时,由固体质量在减小,则草酸亚铁分解生成的是氧化亚铁和一氧化碳、二氧化碳,
FeC2O4
| ||
144 72
0.8g y
解得y=0.4g,
则214℃~280℃发生草酸亚铁分解分解反应,280℃分解完全;
218℃~943℃内由图象可知,固体质量增加,发生的反应是氧化亚铁被氧化为氧化铁,
4FeO+O2═2Fe2O3
288 320
0.4g z
解得z=0.43,
即218℃~943℃内发生化合反应,
答:加热到50℃不发生反应,加热到100℃~214℃时发生失去结晶水的反应使质量减小,214℃~280℃发生分解反应使固体质量减小,280℃~943℃发生化合反应使固体质量增加.

练习册系列答案
相关题目
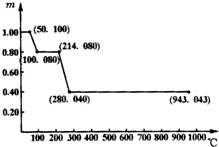 将固体草酸锰MnC2O4?2H2O放在一个可以称出质量的容器里加热.固体质量随温度的变化的关系如图所示,试通过对该图象数据分析和计算,回答在不同温度范围固体质量变化的原因.
将固体草酸锰MnC2O4?2H2O放在一个可以称出质量的容器里加热.固体质量随温度的变化的关系如图所示,试通过对该图象数据分析和计算,回答在不同温度范围固体质量变化的原因.

 CO(g)+2H2(g);△H= -36kJ/mol ①
CO(g)+2H2(g);△H= -36kJ/mol ①  CO(g)+3H2(g);△H= +216kJ/mol ②
CO(g)+3H2(g);△H= +216kJ/mol ②  Na2FeO2+H2O+NH3↑ ①;
Na2FeO2+H2O+NH3↑ ①; 4Na2Fe2O4+3NH3↑ ②;
4Na2Fe2O4+3NH3↑ ②;
