题目内容
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.
单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:

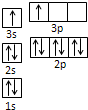
(1)某同学根据上述信息,推断B的核外电子排布如图所示,

该同学所画的电子排布图违背了________.
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为________.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45 pm,C60中C-C键长为145~140 pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确________,并阐述理由________.
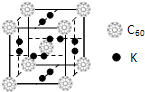
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.写出基态钾原子的电子排布式________,该物质的K原子和C60分子的个数比为________.

(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是________.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为________.
解析:
|
(1)能量最低原理(1分) (2)直线型(1分) (3)不正确(1分) C60是分子晶体,熔化时不需破坏化学键(1分) (4)1s22s22p63s23p64s1(1分) 3∶1(1分) (5)N、C、Si(2分) 30(2分) |

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案(12分)氢气、纳米技术制成的金属燃料、非金属固体燃料已应用到社会生活和高科技领域。
⑴已知短周期金属元素A和B,其单质单位质量的燃烧热大,可用作燃料。其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 899.5 | 1757.1 | 14848.7 | 21006.6 |
| B | 738 | 1451 | 7733 | 10540 |
①根据上述数据分析, B在周期表中位于 区,其最高价应为 ;
②若某同学将B原子的基态外围电子排布式写成了ns1np1,违反了 原理;
③B元素的第一电离能大于Al,原因是 ;
⑵氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由 。
②C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子相对稳定结构,则C60分子中σ键与π键的数目之比为 。
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
(1)某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了????????? 。

(2)ACl2分子中A的杂化类型为???????? 。
(3)我国部分城市雾霾天占全年一半,引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等,其中SO42-的空间构型是??????????? (用文字描述),与NO3-互为等电子体的分子是?????????? 。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物, 其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式????????? ,该物质的K原子和C60分子的个数比为?????????? 。

(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是?????????? 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为?????? 。
 (1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示: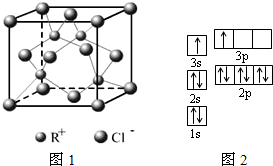 (1)下列是部分金属元素的电离能
(1)下列是部分金属元素的电离能