题目内容
(14分)某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如图所示),大大地提高了资源利用率,减少了环境污染。
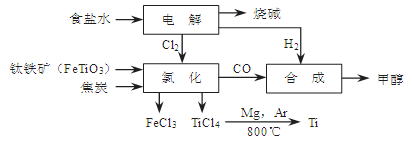
请填写下列空白:
(1)写出钛铁矿经氯化得到四氯化钛的化学方程式: 。
(2)由CO和H2合成甲醇是放热的,方程式是:CO(g)+2H2(g)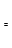 CH3OH(g)。
CH3OH(g)。
①已知该反应在300℃时的化学平衡常数为0.27,该温度下将2 mol CO、3 mol H2和2 mol CH3OH充入容积为2 L的密闭容器中,此时反应将 (填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
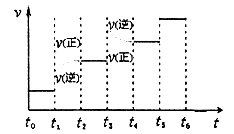
②下图表示合成甲醇反应达到平衡后,每次只改变温度、压强、催化剂中的某一条件,反应速率υ与时间t的关系。其中表示平衡混合物中的甲醇的含量最高的一段时间是 。图中t3时改变的条件可能是 。
(3)某同学设计了一个甲醇燃料电池,并用该电池电解200mL—定浓度NaCl与CuSO4混合溶液,其装置如图:
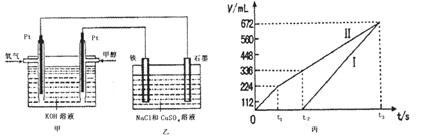
①写出甲中通入甲醇这一极的电极反应式 。
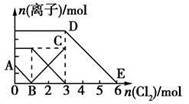
②理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式 ,原混合溶液中NaCl的物质的量浓度为 mol/L。(假设溶液体积不变)

请填写下列空白:
(1)写出钛铁矿经氯化得到四氯化钛的化学方程式: 。
(2)由CO和H2合成甲醇是放热的,方程式是:CO(g)+2H2(g)
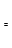 CH3OH(g)。
CH3OH(g)。①已知该反应在300℃时的化学平衡常数为0.27,该温度下将2 mol CO、3 mol H2和2 mol CH3OH充入容积为2 L的密闭容器中,此时反应将 (填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
②下图表示合成甲醇反应达到平衡后,每次只改变温度、压强、催化剂中的某一条件,反应速率υ与时间t的关系。其中表示平衡混合物中的甲醇的含量最高的一段时间是 。图中t3时改变的条件可能是 。

(3)某同学设计了一个甲醇燃料电池,并用该电池电解200mL—定浓度NaCl与CuSO4混合溶液,其装置如图:

①写出甲中通入甲醇这一极的电极反应式 。
②理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式 ,原混合溶液中NaCl的物质的量浓度为 mol/L。(假设溶液体积不变)
⑴ 2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO(2分)
⑵① 向逆反应方向进行(2分)
②t2~t3 (2分)升高温度 (2分)
(3)①CH3OH-6e-+8OH-=CO32-+6H2O(2分)
②4OH--4e-=O2↑+2H2O (2分) 0.1(2分)
⑵① 向逆反应方向进行(2分)
②t2~t3 (2分)升高温度 (2分)
(3)①CH3OH-6e-+8OH-=CO32-+6H2O(2分)
②4OH--4e-=O2↑+2H2O (2分) 0.1(2分)
试题分析:⑴据流程图,钛铁矿氯化过程中反应物有FeTiO3、C、Cl2、,生成物有FeCl3、TiCl4、CO,然后根据氧化还原反应的配平方法将其配平。
⑵①此时该反应的浓度商Qc=
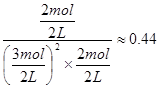 >0.27(K),说明反应向逆反应方向进行;
>0.27(K),说明反应向逆反应方向进行;②结合反应[CO(g)+2H2(g)
 CH3OH(g),正反应放热],并据图可确定“t1~t2”是加压,“t3~t4”是加热(升高温度),“t5~t6”是加催化剂;在t2~t3时间段内平衡混合物中的甲醇的含量最高。
CH3OH(g),正反应放热],并据图可确定“t1~t2”是加压,“t3~t4”是加热(升高温度),“t5~t6”是加催化剂;在t2~t3时间段内平衡混合物中的甲醇的含量最高。⑶①装置甲为甲醇燃料电池,通入甲醇一极为负极,先根据得失电子守恒有CH3OH-6e-――CO32-,再根据电荷守恒有CH3OH-6e-+8OH―――CO32-,最后根据原子守恒得CH3OH-6e-+8OH-=CO32-+6H2O。
②装置乙为电解池,铁电极为阴极,该极发生的电极反应依次为Cu2++2e-=Cu,2H++2e-=H2↑;石墨为阳极,该极发生的电极反应式依次为2Cl--2e-=Cl2↑,4OH--4e-=O2↑+2H2O;据此可确定在t1后,石墨电极上的电极反应式为4OH--4e-=O2↑+2H2O;根据在t1前发生的电极反应“2Cl--2e-=Cl2↑”可计算原混合溶液中NaCl的物质的量浓度:
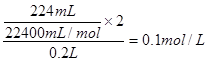 。
。
练习册系列答案
相关题目
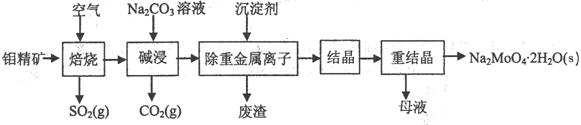 (1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
(1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
 Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。
Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。

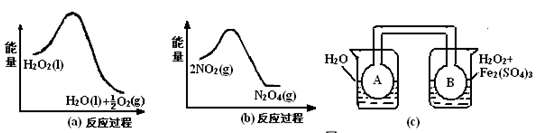
 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1 2CO2(g);ΔH 2
2CO2(g);ΔH 2