题目内容
下列实验事实不能用平衡移动原理解释的是( )
A. | ||||||||
B.
| ||||||||
C.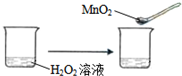 | ||||||||
D.
|
A.存在平衡2NO2?N2O4,且正反应是放热反应,升高温度,平衡向逆反应方向移动,所以气体颜色加深,可以用平衡移动原理来解释,故A不选;
B.水是弱电解质,存在电离平衡H2O?H++OH-,电离过程是吸热过程,升高温度,促进水的电离,氢离子与氢氧根离子的浓度增大,水的离子积中增大,可以用平衡移动原理解释,故B不选;
C.过氧化氢分解,加入的二氧化锰起催化剂的作用,加快过氧化氢分解,不能用平衡移动原理解释,故C选;
D.氨水中存在平衡NH3?H2O?NH4++OH-,浓度越稀,电离程度越大,故0.1mol/L的氨水稀释10倍,pH变化小于1个单位,可以用平衡移动原理解释,故D不选;
故选C.
B.水是弱电解质,存在电离平衡H2O?H++OH-,电离过程是吸热过程,升高温度,促进水的电离,氢离子与氢氧根离子的浓度增大,水的离子积中增大,可以用平衡移动原理解释,故B不选;
C.过氧化氢分解,加入的二氧化锰起催化剂的作用,加快过氧化氢分解,不能用平衡移动原理解释,故C选;
D.氨水中存在平衡NH3?H2O?NH4++OH-,浓度越稀,电离程度越大,故0.1mol/L的氨水稀释10倍,pH变化小于1个单位,可以用平衡移动原理解释,故D不选;
故选C.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目