题目内容
某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如右(写出最佳答案)
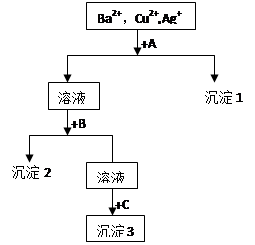
(1)沉淀的化学式:沉淀1 ,沉淀2 ,沉淀3 ;
(2)写出混合液+A的离子方程式 ;
溶液+B的离子方程式 。

(1)沉淀的化学式:沉淀1 ,沉淀2 ,沉淀3 ;
(2)写出混合液+A的离子方程式 ;
溶液+B的离子方程式 。
(1)AgCl Cu(OH)2 BaSO4(每空2分)
(2)Ag+ + Cl- = AgCl↓
Cu2+ + 2OH- = Cu(OH)2↓(每空3分)
(2)Ag+ + Cl- = AgCl↓
Cu2+ + 2OH- = Cu(OH)2↓(每空3分)
试题分析:(1)对含有Ba2+,Cu2+,Ag+的溶液,应先加入HCl,生成AgCl沉淀,过滤后再加入NaOH,可得到Cu(OH)2沉淀,过滤,最后加入Na2SO4,可得到BaSO4沉淀,故A、B、C分别为HCl、NaOH和Na2SO4 沉淀1、沉淀2、沉淀3分别为AgCl 、Cu(OH)2 、BaSO4,(2)混合液+A的离子方程式为Ag+ + Cl- = AgCl↓,溶液+B的离子方程式为Cu2+ + 2OH- = Cu(OH)2↓。
点评:本题考查离子方程式的书写,题目难度中等,注意使离子逐一沉淀应先加入HCl,不能先加入NaOH,否则不能达到逐一沉淀的目的。

练习册系列答案
相关题目
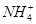 、
、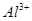 、
、 ,且
,且
 、
、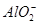 、
、
 、
、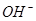 ,且
,且
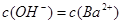
 、
、 、
、 等离子中的若干种。现做如下实验:
等离子中的若干种。现做如下实验:

 SO
SO