题目内容
向含有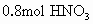 的稀硝酸溶液中慢慢加入22.4g的铁粉.假设反应分
的稀硝酸溶液中慢慢加入22.4g的铁粉.假设反应分
为两个阶段.第一阶段为: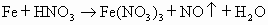
(1)写出这两个阶段反应的离子方程式.
(2)求这两个阶段反应中,加入铁粉的物质的量和溶液中铁元素存在的形式.
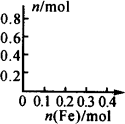
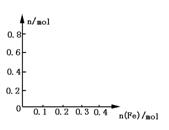
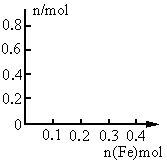
(3)在图中画出溶液中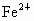 、
、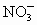 离子的物质的量随加入铁粉的物质的量变化的关系图像(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量).
离子的物质的量随加入铁粉的物质的量变化的关系图像(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量).
答案:略
解析:
解析:
|
(1) 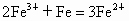
(2) ①加入铁粉为0~0.2mol,为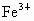 ;②加入铁粉为0.2mol~0.3mol,为 ;②加入铁粉为0.2mol~0.3mol,为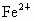 和 和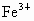 ;③加入铁粉n(Fe)≥0.3mol,为 ;③加入铁粉n(Fe)≥0.3mol,为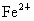 . .
(3) 如图.
有关反应为
当 n(Fe)介于0~0.2mol,仅发生反应①,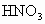 有剩余.生成 有剩余.生成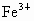 ;当n(Fe)介于0.2~0.3mol时,反应①②同时发生,Fe、 ;当n(Fe)介于0.2~0.3mol时,反应①②同时发生,Fe、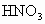 耗尽,生成 耗尽,生成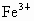 、 、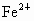 ;当n(Fe)大于0.3mol时,反应①②均发生,Fe有剩余,只生成 ;当n(Fe)大于0.3mol时,反应①②均发生,Fe有剩余,只生成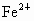 . . |

练习册系列答案
相关题目
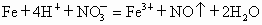
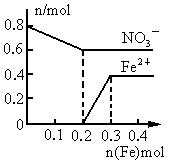
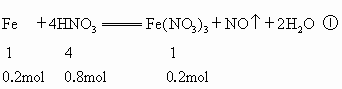
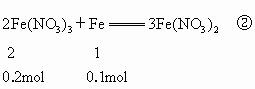
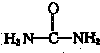 )与NO2-在酸性条件下反应生成两种无毒气体.该反应中生成16.8L(已折算为标准状况)混合气体时,消耗尿素的质量为
)与NO2-在酸性条件下反应生成两种无毒气体.该反应中生成16.8L(已折算为标准状况)混合气体时,消耗尿素的质量为