题目内容
(5分)(1)在一密闭容器中充入1molNO2,建立如下平衡:2NO2 N2O4,测得NO2的转化率为a%,在其它条件不变的情况下,再充入1molNO2,待新平衡建立时,又测得NO2的转化率为b%。试问a、b值的大小关系为___ _。
(2)汽车尾气中的主要污染物有CO、NOx ,CO分析仪是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是 。
A.负极的电极反应式为:CO+O2—―2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,说明汽车尾气中CO的含量越高
(3)阿波罗宇宙飞船上使用的是氢氧燃料电池,试回答下列问题:
①若电解质溶液为KOH溶液,构成燃料电池,则负极反应式为____________ ____,
②如把KOH改为稀H2SO4作电解质,则正极反应式为_____ ___________,
③如把H2改为甲烷,KOH作电解质,则负极反应式为
(1)b>a (2)B (3) ①2H2+4OH--4e-===4H2O ② O2+4H++4e-===2H2O ③ CH4-8e-+10OH-=CO32-+7 H2O
解析:(1)由于反应物和生成物都是一种,所以再通入NO2相当于增大压强,平衡向正反应方向移动,转化率增大。原电池中阳离子向正极移动,阴离子向负极移动。根据装置图可判断,a是负极,CO被氧化。b是正极,氧气被还原。所以选项B是错误的。(3)负极失去电子,所以氢气通入负极,氧气通入正极。若用甲醇作燃料,则甲醇在负极失去电子,由于溶液是氢氧化钾溶液,所以生成物是碳酸钾和水。

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【实验Ⅰ】制取NaNO2
该小组查阅资料知:2NO+Na2O2═2NaNO2;2NO2+Na2O2═2NaNO3设计割取装置如下(夹持装置略去):
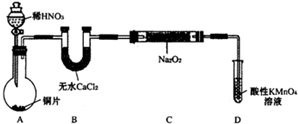
(1)装置D可将剩余的NO氧化成N03,发生反应的离子方程式为
(2)如果没有B装置,C中发生的副反应有
(3)甲同学梭在完气密往良好后进行实验,发现NaNO2的纯度较低.乙简学对上述装置进行了改进后提高了NaNO2的纯度,其改进措施是
(4)丙同学撩B中的药品进行了更换,也提高了NaNO2鲍纯度.丙更换的药最是
【实验Ⅱ】测定甲、乙同学制取样晶中NaNO2的含量
步骤:a.在5个有编号的带刻度试管(比色管)中分别加入不同量的NaNO2溶液,各加入1mL的M溶液(M遇NaN02呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10mL并振荡,制成标准色阶:
| 试管编号 | ① | ② | ③ | ④ | ⑤ |
| NaNO2含量/mg?L-1 | 0 | 20 | 40 | 60 | 80 |
(5)步骤b中比较结果是:甲待测液颜色与③号色阶相同,乙待测液颜色与④号色阶相同.则甲同学制得的样品中NaN02的纯度是
(6)用目视比色法证明维生素C可以有效降低NaNO2的含量.设计并完成下列实验报告.
| 实验方案 | 实验现象 | 实验结论 |
| 维生素C可以有效降低NaNO2的含量 |
硫酸铜是一种应用极其广泛的化工原料.某课外兴趣小组将适量浓硝酸分多次加到铜粉与稀硫酸的混合物中,加热使之反应完全(装置如图I、图Ⅱ所示),通过蒸发、结晶得到硫酸铜晶体,并同时测定硫酸铜晶体中结晶水的含量.
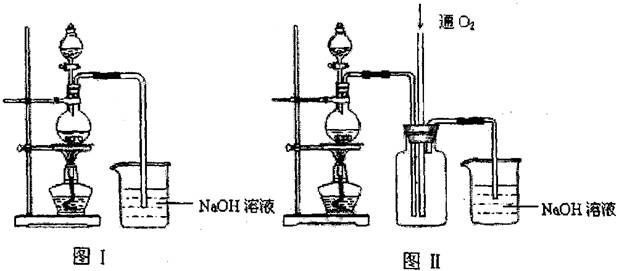
(1)怎样检查图I装置的气密性 。
(2)图I中分液漏斗内装的液体是 。
(3)图Ⅱ是图Ⅰ的改进装置,与图I相比,图Ⅱ装置的明显优点是 ,
, ,(可不答满).
(4)课外兴趣小组同学在测定胆矾(CuSO4·χH2O)晶体中结晶水的含量时.测得有关数据如下表:
|
加热前质量 |
加热后质量 |
|
|
m1(容器) |
m2(容器+晶体) |
m3(容器+无水CuSO4) |
|
5.4g |
7.9g |
6.8g |
①为完成测定,图Ⅲ中还缺少的仪器名称是 。
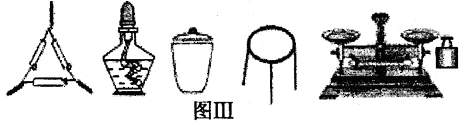
②判断样品已恒重的方法是 。
③测定所得胆矾(CuSO4·χH2O)中结晶水含量的实验中,称量操作至少进行 次。
④课外兴趣小组的测定结果x值(与CuSO4·5H2O相比) (填“偏高”、“偏低”、“不变”),可能的原因是 。(填字母序号)
a.加热温度过高
b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却
d.胆矾晶体部分风化
|
学校 姓名 考号 班级
|
|
……………………………………………密………………………………………封……………………………………………….线………………………………………………….
|
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
| A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
| B元素原子的核外p电子总数比s电子总数少1 |
| C原子p轨道上成对电子数等于未成对电子数,且与A同周期 |
| D元素的族序数与周期数的差为4,且不与A元素在同一周期 |
| E位于周期表中第七列 |
| F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
(1)A的基态原子最外层有 种不同运动状态的电子,F位于 区。
(2)E2+的基态核外电子排布式为 ,AD4为 (填极性或非极性)分子。
(3)A、B、C三种元素的电负性由小到大的顺序是 (用元素符号表示),B和C两元素中,B的第一电离能较大的原因是 ,与AC2互为等电子体的分子的名称为 。(只写一种)
(4)BD3 中心原子的杂化方式为 ,其分子空间构型为 。
(5)用晶体的x射线衍射法对F的测定得到以下结果:F的晶胞为
面心立方最密堆积(如右图),又知该晶体的密度为ρg/cm3,
晶胞中该原子的配位数为 ;F的原子半径是 pm;
(阿伏加德罗常数为NA)。

