题目内容
下列实验原理、装置、试剂选用、结论正确的是
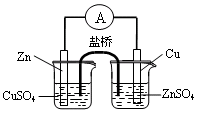
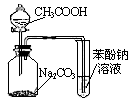
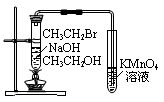
图1 图2 图3
| A.用湿润的pH试纸测定稀盐酸的pH |
| B.用下图1构成锌—铜原电池 |
| C.用下图2根据有关实验现象推知酸性:CH3COOH>H2CO3>C6H5OH |
| D.用下图3验证溴乙烷发生消去反应生成烯烃 |



图1 图2 图3
C
A 错误,检测溶液的PH值时,pH试纸不能润湿
B 错误,左右两个烧杯的溶液颠倒一下。
C 正确,强酸制弱酸
D 错误,挥发出的乙醇蒸气也能是高锰酸钾褪色。
B 错误,左右两个烧杯的溶液颠倒一下。
C 正确,强酸制弱酸
D 错误,挥发出的乙醇蒸气也能是高锰酸钾褪色。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

 H)2可以溶于稀氨水生成可溶性的Zn(NH3)4(OH)2;下列是该同学对操作②的滤液主次成分进行探究的过程:
H)2可以溶于稀氨水生成可溶性的Zn(NH3)4(OH)2;下列是该同学对操作②的滤液主次成分进行探究的过程: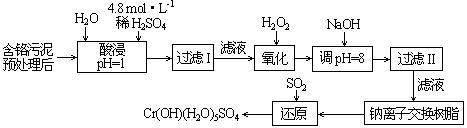
 主要成分是氯气,还含有少量空气和水蒸气。
主要成分是氯气,还含有少量空气和水蒸气。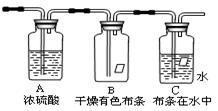
 CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
 接顺序(按产物气流从左到右的方向)是(填装置的编号):
接顺序(按产物气流从左到右的方向)是(填装置的编号): ④ →__________→__________→__________。
④ →__________→__________→__________。 增重质量为bg。用a、b表示CO2和SO2的物质的量比 。
增重质量为bg。用a、b表示CO2和SO2的物质的量比 。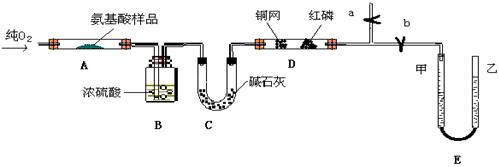
 的硝酸银溶液
的硝酸银溶液 是称量和 ,在实验中需要测定的数据有 。
是称量和 ,在实验中需要测定的数据有 。