题目内容
事实上,许多氧化物在一定条件下能与Na2O2反应,且反应极有规律,如Na2O2 +SO2 →Na2SO4;2Na2O2 +2SO3→2Na2SO4 +O2 ,据此你认为下列反应方程式中正确的是
| A.2Na2O2 + 2N2O3→4NaNO2 + O2 | B.Na2O2 + 2NO2 →2NaNO2 + O2 |
| C.Na2O2 + N2O4→2NaNO3 | D.2Na2O2 + 2 Mn2O7 → 4NaMnO4 + O2 |
CD
试题分析:A、根据已知反应可知,当非金属氧化物中非金属元素的化合价处于最高价时,与过氧化钠反应生成氧气,否则得不到氧气。N2O3中N元素的化合价为+3价,不是最高价态,与Na2O2反应时不生成O2,故A错误;B、NO2中N元素的化合价为+4价,不是最高价态,与Na2O2反应时不生成O2,反应的化学方程式为Na2O2+2NO2=2NaNO3,故B错误;C、N2O4中N元素的化合价为+4价,不是最高价态,与Na2O2反应时不生成O2,反应的化学方程式为Na2O2+N2O4→2NaNO3,故C正确;D、Mn2O7中Mn元素的化合价为+7价,处于最高价态,与Na2O2反应时生成O2,故D正确,答案选CD。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
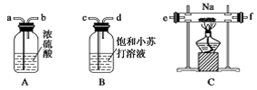
 变灰暗
变灰暗 变白色
变白色 出现液滴
出现液滴 白色固体,
白色固体,