题目内容
在一定温度下将1 mol CO和1 mol水蒸气放入一固定容积的密闭容器中,反应CO(g)+H2O? ?CO2(g)+H2(g)达平衡后,得到0.6 mol CO2;再通入0.3 mol水蒸气,达到新平衡状态后,CO2的物质的量可能是( )
?CO2(g)+H2(g)达平衡后,得到0.6 mol CO2;再通入0.3 mol水蒸气,达到新平衡状态后,CO2的物质的量可能是( )
A.0.9 mol B.0.7 mol C. 0.8 mol D.0.6 mol
【答案】
C
【解析】再通入0.3 mol水蒸气,平衡向正反应方向移动,水蒸气的转化量降低,即转化率小于60%。所以CO2的物质的量一定是大于0.6mol,但小于1.3mol×60%=0.78mol,答案选B。

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
 在一定温度下,将两种气体M和N通入容积为V L的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法不正确的是( )
在一定温度下,将两种气体M和N通入容积为V L的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法不正确的是( )| A、t2时M与N的物质的量浓度之比为1:1 | ||
| B、t2与t3时刻的混合气体的平均相对分子质量相等 | ||
| C、反应物与生成物平衡时的物质的量浓度之比是2:5 | ||
D、0~t2内用M表示的平均反应速率是
|
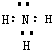
 HCO3-+OH-
HCO3-+OH- 在一定温度下,在容积为2L的容器内,某反应各物质(均为气体)的物质的量随反应时间的变化曲线如图,试回答下列问题:
在一定温度下,在容积为2L的容器内,某反应各物质(均为气体)的物质的量随反应时间的变化曲线如图,试回答下列问题: M
M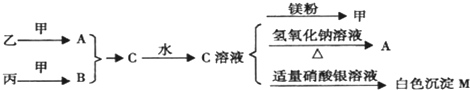
 (1)1mol O2与足量氢气反应产生水蒸气放热483.6kJ,若1g水蒸气转化成液态水放热2.444kJ,请写出表示氢气燃烧热的热化学方程式:
(1)1mol O2与足量氢气反应产生水蒸气放热483.6kJ,若1g水蒸气转化成液态水放热2.444kJ,请写出表示氢气燃烧热的热化学方程式: