题目内容
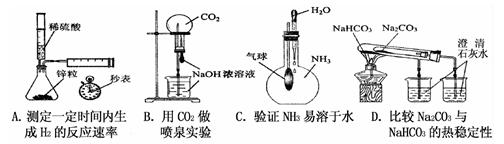
如图是课外活动小组同学设计的4个喷泉实验方案.下列有关操作不可能引发喷泉现象的是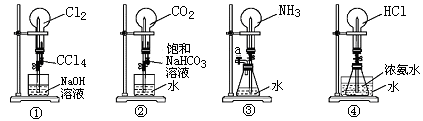
| A.挤压装置①的胶头滴管使CCl4全部进人烧瓶,片刻后打开止水夹 |
| B.挤压装置②的胶头滴管使饱和NaHCO3溶液全部进人烧瓶.片刻后打开止水夹 |
| C.用鼓气装置从装置③的a处不断鼓人空气并打开止水夹 |
| D.向装置④的水槽中慢慢加人足量浓硫酸并打开止水夹 |
B
解析试题分析:能否产生喷泉现象关键要看能否产生压强差,A中氯气易溶于四氯化碳,且又能和氢氧化钠反应,故可以。B中二氧化碳在饱和NaHCO3溶液不溶难以产生压强差,不能形成喷泉。C氨气是极易溶于水,能形成喷泉。D加人足量浓硫酸会与水放热加速氨气挥发,氨气能和氯化氢反应生成固体氯化铵形成压强差,形成喷泉。
考点:本题考查了喷泉形成的原理。

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
一些化学试剂瓶上贴有危险警告标志,下列物质的试剂瓶上所贴化学品标志有错误的是
| | A | B | C | D |
| 物质 | NaHCO3 | 黑火药 | 浓H2SO4 | KMnO4 |
| 危险警告标识 |  |  |  |  |
在非室温条件下可以使用的仪器是
| A.漏斗 | B.量筒 | C.容量瓶 | D.滴定管 |
下列溶液配制实验的描述完全正确的是
| A.在容量瓶中先加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸 |
| B.用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol.L-1)通常需要用容量瓶等仪器 |
| C.配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4以防水解 |
| D.用PH=1的盐酸配制100mL, PH=2的盐酸所需全部玻璃仪器有100mL容量瓶、烧杯、玻璃棒、胶头滴管 |
下列有关试剂的保存方法,错误的是
| A.氢氟酸保存在无色玻璃试剂瓶中 |
| B.氢氧化钠溶液保存在具橡皮塞的玻璃试剂瓶中 |
| C.少量的钠保存在煤油中 |
| D.新制的氯水通常保存在棕色玻璃试剂瓶中 |
下列实验方案不可行或结论不正确的是
| A.用润湿的pH试纸测定饱和Na2CO3溶液pH |
| B.通过观察图中导管水柱的变化,验证铁钉生锈的原因主要是吸氧腐蚀 |
| C.向Mg(OH)2悬浊液中滴加FeCl3溶液,出现红褐色沉淀,说明溶解度:Fe(OH)3<Mg(OH)2 |
| D.向同pH、同体积的醋酸和盐酸溶液中加入足量镁粉,通过完全反应后收集到的H2体积比较两种酸的电离程度:醋酸<盐酸 |
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是
| A.所用NaOH已吸潮 |
| B.向容量瓶加水时液面低于刻度线即摇匀 |
| C.有少量NaOH溶液残留在烧杯内 |
| D.向容量瓶加水时眼睛一直仰视液面 |