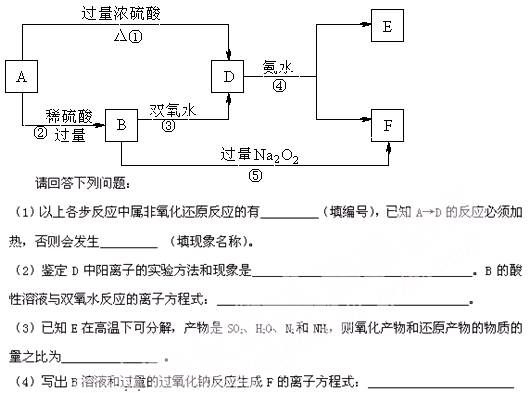
题目内容
某含铬[Cr2O72-] 废水用硫酸亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀.该沉淀干燥后得到n molFeO·FeyCrxO3.不考虑处理过程中的实际损耗,下列叙述错误的是 ( )
| A.消耗硫酸亚铁铵的物质量为n(2-x)mol |
| B.处理废水中Cr2O72-的物质量为mol |
| C.反应中发生转移的电子数为3nx mol |
| D.在FeO·FeyCrxO3中3x=y |
A
答案:A
反应中铁元素和铬元素完全转化为沉淀n mol FeO·FeyCrxO3,由铬原子守恒得B选项正确。1 mol Cr2O72-在反应中得6 mol 电子,1 mol Cr2O72-反应中转移的电子数为6×1mol = 3nx mol,C选项正确。沉淀中FeO的化合价没有变化,由得失电子守恒得3nx=ny, 3x=y D选项正确。而由铁元素守恒知消耗硫酸亚铁铵的物质量为n×(1+y)mol = n×(3x+1)mol,因此选项A是错误的。

练习册系列答案
相关题目

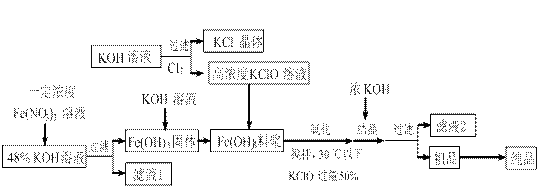
 ▲ 。
▲ 。 O3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ▲ 。
O3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ▲ 。

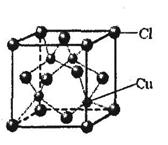
 应中其它产物未列出):
应中其它产物未列出):