题目内容
某教师在上《元素周期表》复习课时,组织了一个“介绍自己”的活动:
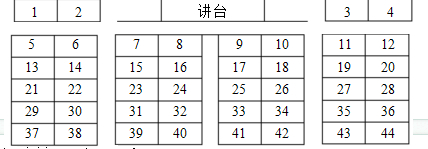
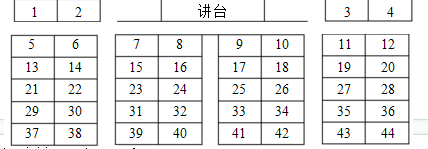
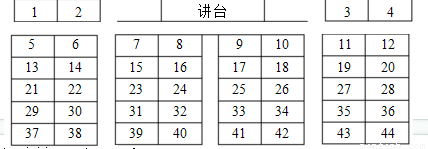
我们班级中共有44位同学,分为8个小组(学生座位如图所示,数字表示座位号),按从左到右分别为IA、IIA……VIIA、0族,从上到下分别为第一、二……六周期。座位上的每一位同学对应一种元素,请在下列问题中符合要求的同学向大家介绍自己。
|
|
2 |
|
|
讲 台 |
|
|
3 |
|
||||
|
5 |
6 |
7 |
8 |
|
9 |
10 |
11 |
12 |
||||
|
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|||||
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
|||||
|
29 |
30 |
31 |
32 |
33 |
34 |
35 |
36 |
|||||
|
37 |
38 |
39 |
40 |
41 |
42 |
43 |
44 |
请你一起思考并回答下列问题:
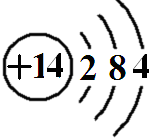
(1)第三周期IVA族的元素对应座位号是 ,原子结构示意图为 。
(2)座位号为22的元素在元素周期表中的位置是 。
(3)比较座位号为18、19对应的元素的非金属性强弱,请用离子方程式表示 。
(4)课堂中有学生提出,这样的安排会导致他们没有对应的元素,则学生对应的座位号是 。
(1)16(1分),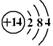 (1分) (2)第四周期IIA族(1分)
(1分) (2)第四周期IIA族(1分)
(3)Cl2+S2-=S↓+2Cl-或Cl2+H2S=2H++S↓+2Cl-(2分) (4)2,3(2分)
【解析】考查元素周期表的结构。
(1)第三周期IVA族的元素是硅,原子序数为14,所以对应的是16,原子结构示意图为 。
。
(2)座位号为22的元素是钙元素,位于第四周期IIA族。
(3)座位号为18、19对应的元素分别是S和Cl,同周期自左向右 非金属性直接增强,所以氯元素的强于硫的。比较元素非金属性强弱可用单质之间的相互置换来验证,即Cl2+S2-=S↓+2Cl-或Cl2+H2S=2H++S↓+2Cl-。
(4)由于 第一周期中只有元素H和He,所以座位号是2、3的没有对应的元素。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案某教师在上《元素周期表》复习课时,组织了一个“介绍自己”的活动:
我们班级中共有44位同学,分为8个小组(学生座位如图所示,数字表示座位号),按从左到右分别为IA、IIA……VIIA、0族,从上到下分别为第一、二……六周期。座位上的每一位同学对应一种元素,请在下列问题中符合要求的同学向大家介绍自己。
| 2 | | | 讲 台 | | | 3 |
| ||||||
| 5 | 6 | 7 | 8 | | 9 | 10 | 11 | 12 | ||||||
| 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | |||||||
| 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | |||||||
| 29 | 30 | 31 | 32 | 33 | 34 | 35 | 36 | |||||||
| 37 | 38 | 39 | 40 | 41 | 42 | 43 | 44 | |||||||
(1)第三周期IVA族的元素对应座位号是 ,原子结构示意图为 。
(2)座位号为22的元素在元素周期表中的位置是 。
(3)比较座位号为18、19对应的元素的非金属性强弱,请用离子方程式表示 。
(4)课堂中有学生提出,这样的安排会导致他们没有对应的元素,则学生对应的座位号是 。