题目内容
13、能与氢氧化钠溶液反应的原子晶体是( )
A、铝 B、金刚石 C、硅 D、二氧化硅
CD
解析:铝与氢氧化钠溶液反应生成NaAlO2是离子晶体。硅、二氧化硅与氢氧化钠溶液反应,而且是原子晶体,CD正确。金刚石与氢氧化钠溶液不反应

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
应用元素周期律分析下列推断,其中正确的组合是( )
①铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
②气态氢化物的稳定性HF大于HCl
③硒(Be)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性.
①铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
②气态氢化物的稳定性HF大于HCl
③硒(Be)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性.
| A、①③ | B、②④ | C、①④ | D、②③ |
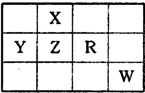 图为元索周期表前四周期的一部分,且X、Y、Z、R和W为主族元素.下列说法正确的是( )
图为元索周期表前四周期的一部分,且X、Y、Z、R和W为主族元素.下列说法正确的是( )| A、Y单质一定既能与盐酸又能与氢氧化钠溶液反应 | B、五种元素的原子最外层电子数一定都大于2 | C、单质X的熔点一定比单质Z的熔点高 | D、R的最高价氧化物对应的水化物一定是强酸 |