题目内容
(2009?茂名一模)X、Y、Z、W为四种短期周期主族元素.其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高价与最低负价的代数和为6.下列说法正确的是( )
分析:X原子最外层电子数是核外电子层数的3倍,则X为O元素,X、Z同族,则Z为S元素,Y的最高正价与最低负价的代数和为6,则Y的最高价为+7价,为第VIIA族元素,且与硫同周期,所以Y为Cl元素,W为H元素,结合元素周期律的递变规律来分析解答.
解答:解:X原子最外层电子数是核外电子层数的3倍,则X为O元素,X、Z同族,则Z为S元素,Y的最高正价与最低负价的代数和为6,则Y的最高价为+7价,为第VIIA族元素,且与硫同周期,所以Y为Cl元素,W为H元素,
A.元素周期表中,同周期元素从左到右原子半径逐渐减小,同主族元素从上到下,原子半径逐渐增大,则原子半径由小到大的顺序为H<O<Cl<S,故A错误;
B.Y是Cl元素,Z是S元素,同一周期中,元素的非金属性随着原子序数的增大而增强,元素的非金属性越强,其阴离子的还原性越弱,所以Y、Z两元素形成的简单阴离子的还原性Z>Y,故B正确;
C.O是H元素,W是H元素,X与W形成的化合物H2O2中含有极性共价键和非极性共价键,不含离子键,故C错误;
D.X是O元素,Z是S元素,O元素没有最高价氧化物的水化物,故D错误;
故选B.
A.元素周期表中,同周期元素从左到右原子半径逐渐减小,同主族元素从上到下,原子半径逐渐增大,则原子半径由小到大的顺序为H<O<Cl<S,故A错误;
B.Y是Cl元素,Z是S元素,同一周期中,元素的非金属性随着原子序数的增大而增强,元素的非金属性越强,其阴离子的还原性越弱,所以Y、Z两元素形成的简单阴离子的还原性Z>Y,故B正确;
C.O是H元素,W是H元素,X与W形成的化合物H2O2中含有极性共价键和非极性共价键,不含离子键,故C错误;
D.X是O元素,Z是S元素,O元素没有最高价氧化物的水化物,故D错误;
故选B.
点评:本题考查了元素位置结构关系的应用,根据其结构关系来确定元素,并结合元素周期律来分析解答,难度中等.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
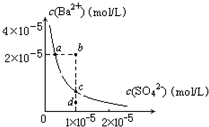 (2009?茂名一模)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是(提示BaSO4(s)?Ba2+(aq)+SO42-(aq)的平衡常数Ksp=[Ba2+]?[SO42-],称为溶度积常数)( )
(2009?茂名一模)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是(提示BaSO4(s)?Ba2+(aq)+SO42-(aq)的平衡常数Ksp=[Ba2+]?[SO42-],称为溶度积常数)( )



