题目内容
在高温下反应 2HBr(g)═H2(g)+Br2(g),△H>0达到平衡时要使混合气体颜色加深,可采取的方法是( )
分析:要使混合气体的颜色加深,应使c(Br2)增大,可使平衡向正反应方向移动,缩小容器的体积、升高温度等.
解答:解:A、减小压强平衡不移动,但体积增大,c(Br2)减小,混合气体的颜色变浅,故A错误;
B、缩小体积,压强增大,平衡不移动,c(Br2)增大,混合气体的颜色变深,故B正确;
C、该反应正反应是吸热反应,升高温度,平衡向正反应移动,c(Br2)增大,混合气体的颜色变深,故C正确;
D、增大氢气的浓度,平衡向逆反应移动,c(Br2)减小,混合气体的颜色变浅,故D错误;
故选BC.
B、缩小体积,压强增大,平衡不移动,c(Br2)增大,混合气体的颜色变深,故B正确;
C、该反应正反应是吸热反应,升高温度,平衡向正反应移动,c(Br2)增大,混合气体的颜色变深,故C正确;
D、增大氢气的浓度,平衡向逆反应移动,c(Br2)减小,混合气体的颜色变浅,故D错误;
故选BC.
点评:本题考查影响化学平衡的因素,难度不大,注意把握从平衡移动的角度使c(Br2)增大的措施.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


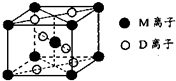 (2013?绵阳模拟)A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大.其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体.
(2013?绵阳模拟)A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大.其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体.
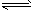 H2(g)+Br2(g),其△H>0,达平衡时,要使混合气体的颜色加深,可采取的方法是
H2(g)+Br2(g),其△H>0,达平衡时,要使混合气体的颜色加深,可采取的方法是