题目内容
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下: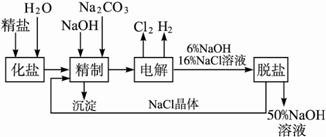
依据上图,完成下列填空:
(1)工业食盐中含Ca2+、Mg2+等杂质,精制过程中发生反应的离子方程式为 ___________________________,___________________________。
(2)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________________。
,该钡试剂可以是________________。
a.Ba(OH)2?b.Ba(NO3)2?c.BaCl2
(3)为有效除去Ca2+、Mg2+、![]() ,加入试剂的合理顺序为____________。
,加入试剂的合理顺序为____________。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______________、冷却、______________除去NaCl。(填写操作名称)
(5)电解食盐水时,总的反应方程式为____________________________。
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为____________________________。
解析:(1)由框图,食盐精制时加入了NaOH和Na2CO3,则Mg2+被OH-除去,Ca2+被![]() 除去。由于S〔Mg(OH)2〕<S(MgCO3),所以不生成MgCO3沉淀。
除去。由于S〔Mg(OH)2〕<S(MgCO3),所以不生成MgCO3沉淀。
(2)![]() 可用Ba2+除去:Ba2++
可用Ba2+除去:Ba2++![]() ══BaSO4↓,但不能选择Ba(NO3)2,因为会引入
══BaSO4↓,但不能选择Ba(NO3)2,因为会引入![]() ,原溶液是NaCl(aq),要制取的是NaOH(aq)(或NaOH),故OH-和Cl-不是杂质。
,原溶液是NaCl(aq),要制取的是NaOH(aq)(或NaOH),故OH-和Cl-不是杂质。
(3)加入过量的钡试剂,而过量的Ba2+必须除去,所以加入钡试剂必须在加入Na2CO3之前,以利用Na2CO3除去Ba2+,Ba2++![]() ══BaCO3↓。
══BaCO3↓。
(4)由于溶解度NaOH>NaCl,而脱盐得到的是NaCl(s)和NaOH(aq),所以可采用先加热蒸发水分——溶解度小的首先析出,再过滤的办法。
(6)如果生成的Cl2与NaOH充分接触,则电解过程中先后发生下列反应:
2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
+)2NaOH+Cl2══NaCl+NaClO+H2O
NaCl+H2O![]() NaClO+H2↑
NaClO+H2↑
答案:(1)Ca2++![]() ══CaCO3↓ Mg2++2OH-══Mg(OH)2↓
══CaCO3↓ Mg2++2OH-══Mg(OH)2↓
(2)ac (3)bc (4)蒸发 过滤
(5)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(6)NaCl+H2O![]() NaClO+H2↑
NaClO+H2↑

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案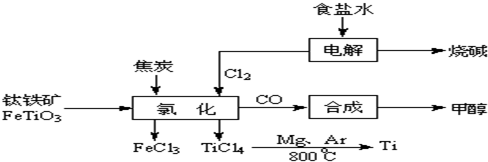
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑ 2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
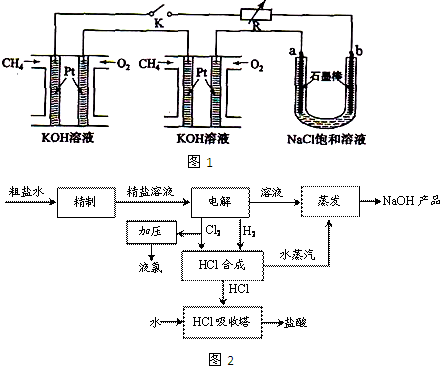




 ____________
____________

 在Ar气氛中进行的理由是________
在Ar气氛中进行的理由是________