题目内容
14.下列反应的离子方程式书写正确的是( )| A. | 锌粒与稀盐酸反应:Zn+2H+=Zn2++H2↑ | |
| B. | 溴化钠溶液与氯气反应:Br-+Cl2=Cl-+Br2 | |
| C. | 氢氧化铜与稀硫酸反应:OH-+H+=H2O | |
| D. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
分析 A.反应生成氯化锌和氢气;
B.原子、电子不守恒;
C.氢氧化铜在离子反应中保留化学式;
D.电子不守恒.
解答 解:A.锌粒与稀盐酸反应的离子反应为Zn+2H+=Zn2++H2↑,故A正确;
B.溴化钠溶液与氯气反应的离子反应为2Br-+Cl2=2Cl-+Br2,故B错误;
C.氢氧化铜与稀硫酸反应的离子反应为Cu(OH)2+2H+=2H2O+Cu2+,故C错误;
D.钠与水反应的离子反应为2Na+2H2O=2Na++2OH-+H2↑,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应的考查,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
4.如图所示装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是( )
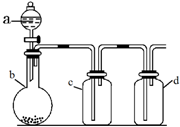

| A. | 若a为浓盐酸,b为MnO2,c中盛品红溶液,则c中溶液褪色 | |
| B. | 若a为醋酸溶液,b为贝壳,c中盛过量澄清石灰水,则c中溶液变浑浊 | |
| C. | 若a为浓硫酸,b为Na2SO3固体,c中盛紫色石蕊溶液,则c中溶液变红 | |
| D. | 若a为浓氨水,b为生石灰,c中盛AlCl3溶液,则c中产生白色沉淀 |
5.实验室制取氯气应该选用哪一套装置( )
| A. | 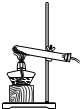 | B. | 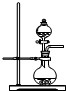 | C. | 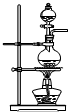 |
9.下列物质中属于含有共价键的离子化合物的是( )
| A. | NaOH | B. | AlCl3 | C. | K2S | D. | Cl2 |
19.在下列有关晶体的叙述中错误的是( )
| A. | 稀有气体的原子能形成分子晶体 | B. | 离子晶体中,一定存在离子键 | ||
| C. | 原子晶体中,只存在共价键 | D. | 金属晶体的熔沸点均很高 |
4.某化学反应过程中的能量变化关系如图所示,下列结论正确的是( )
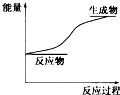

| A. | 生成物的总能量小于反应物的总能量 | |
| B. | 断开化学键所吸收的能量小于形成化学键所放出的能量 | |
| C. | 该反应可能是酸和碱的中和反应 | |
| D. | 该反应中其他形式的能量转化成了化学能 |
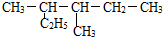 的系统命名:3,4-二甲基已烷
的系统命名:3,4-二甲基已烷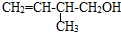 的键线式:
的键线式: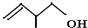
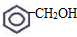 ③
③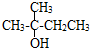 ④
④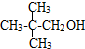 ⑤
⑤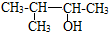 ⑥
⑥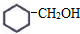
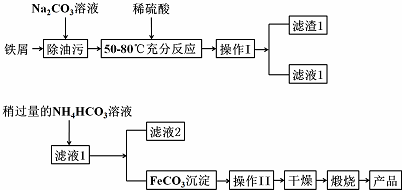
 ;
;