题目内容
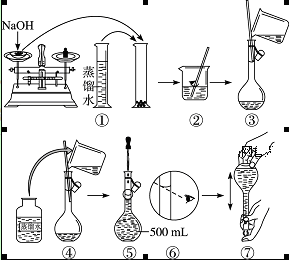
(7分)、某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
② 固定好滴定管并使滴定管尖嘴充满液体
③ 调节液面至“0”或“0”刻度线稍下,并记下读数
④ 移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤ 用标准液滴定至终点,记下滴定管液面读数。
请回答:(1)以上步骤有错误的是(填编号) ,
该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”) ______ ;
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无响”)____________ ;
(3)判断滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟不变色;
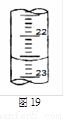
(4)右图是某次滴定时的滴定管中的液面,其读数为 mL;
(5)根据下列数据:请计算待测盐酸溶液的浓度: mol/L。
|
滴定次数 |
待测体积(ml) |
标准烧碱体积(ml) |
|
|
滴定前读数 |
滴定后读数 |
||
|
第一次 |
20.00 |
0.40 |
20.40 |
|
第二次 |
20.00 |
4.00 |
24.00 |
|
第三次 |
20.00 |
2.00 |
24.10 |

【解析】略

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案(12分)配制500 mL 0.5 mol/L的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为________。
(2)本实验必须用到的玻璃实验仪器除容量瓶、烧杯外,还有____________________________。
(3)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放在标尺的零刻度处,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将____________________(填“高于”或“低于”)右边的托盘。假定最终称得小烧杯的质量为____________(填“32.6 g”或“32.61 g”),请用“↓”表示在托盘上放上砝码,“↑”表示从托盘上取下砝码的称量过程。
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 称量(取用砝码)过程 | | | | | |
①向盛有NaOH的烧杯中加入200 mL蒸馏水使其溶解,并冷却至室温。
②继续往容量瓶中加蒸馏水至液面接近刻度线1 cm~2 cm。
③将NaOH溶液沿玻璃棒注入500 mL容量瓶中。
④在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移入容量瓶。
⑤改用胶头滴管加蒸馏水至刻度线,加盖摇匀。
试将以上操作按正确顺序编出序号 。
(5)某学生实际配制NaOH溶液的浓度为0.48 mol/L,原因可能是( )
A.使用滤纸称量氢氧化钠固体
B.容量瓶中原来存有少量蒸馏水
C.溶解后的烧杯未经多次洗涤
D.胶头滴管加水后定容时仰视刻度