题目内容
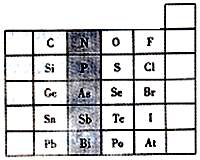
根据元素周期律判断,下列递变规律不正确的是( )
分析:A.同周期自左而右元素金属性减弱;
B.同主族自上而下元素的非金属性减弱,非金属性越强氢化物越稳定;
C.同周期自左而右元素的非金属性增强,非金属性越强最高价含氧酸的酸性越强;
D.同主族自上而下元素的金属性增强,金属单质越活泼.
B.同主族自上而下元素的非金属性减弱,非金属性越强氢化物越稳定;
C.同周期自左而右元素的非金属性增强,非金属性越强最高价含氧酸的酸性越强;
D.同主族自上而下元素的金属性增强,金属单质越活泼.
解答:解:A.同周期自左而右元素金属性减弱,故Na、Mg、Al的金属性依次减弱,故A正确;
B.同主族自上而下元素的非金属性减弱,非金属性Cl>Br>I,非金属性越强氢化物越稳定,故HCl、HBr、HI的稳定性依次减弱,故B错误;
C.同周期自左而右元素的非金属性增强,非金属性Cl>S>P,非金属性越强最高价含氧酸的酸性越强,故HCl04、H2S04、H3P04的酸性依次减弱,故C正确;
D.同主族自上而下元素的金属性增强,故Li、Na、K活泼性增强,故Li、Na、K分别与水反应的剧烈程度依次增强,故D正确;
故选B.
B.同主族自上而下元素的非金属性减弱,非金属性Cl>Br>I,非金属性越强氢化物越稳定,故HCl、HBr、HI的稳定性依次减弱,故B错误;
C.同周期自左而右元素的非金属性增强,非金属性Cl>S>P,非金属性越强最高价含氧酸的酸性越强,故HCl04、H2S04、H3P04的酸性依次减弱,故C正确;
D.同主族自上而下元素的金属性增强,故Li、Na、K活泼性增强,故Li、Na、K分别与水反应的剧烈程度依次增强,故D正确;
故选B.
点评:本题考查同周期同主族元素性质的递变规律,比较基础,注意对规律的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
根据元素周期律判断,下列叙述正确的是( )
| A、酸性强弱:H3PO4>H2SO4 | B、金属性:Na>Al | C、碱性强弱:NaOH<Mg(OH)2 | D、原子半径:Cl>Na |