题目内容
下面4个实验,其中肯定有错误的是( )①有一瓶澄清的碱性溶液,作离子鉴定时得出的结论是含有Ca2+、Fe2+、Na+、Cl-和![]()
②某一固体混合物溶于水后,检验出含K+、![]() 、Na+和Cl-,则该固体混合物是KNO3和NaCl或NaNO3和KCl的混合物
、Na+和Cl-,则该固体混合物是KNO3和NaCl或NaNO3和KCl的混合物
③固体NaOH因部分吸收了空气中的CO2并溶于水后,溶液中会含有较多的![]()
④氯化铁溶液显酸性,某人想使其成为中性溶液, 便向其中加入烧碱溶液
A.①和② B.②和④ C.②和③ D.①③④
解析:①中碱性溶液中不可能有Fe2+,同时![]() 和Ca2+不能共存。③中固体NaOH因部分吸收了空气中的CO2并溶于水后,溶液中会含有较多的
和Ca2+不能共存。③中固体NaOH因部分吸收了空气中的CO2并溶于水后,溶液中会含有较多的![]() 。④中加入烧碱溶液会生成沉淀。答案:D
。④中加入烧碱溶液会生成沉淀。答案:D

 阅读快车系列答案
阅读快车系列答案|
为了探究影响化学反应速率的因素,4位同学分别设计了下列4个实验,其中结论不正确的是 | |
| [ ] | |
A. |
将大小、形状相同的镁条和铝条与相同浓度、相同温度下的盐酸反应时,两者快慢相同 |
B. |
在相同条件下等质量的大理石块和大理石粉与相同浓度的盐酸反应时,粉比块反应快 |
C. |
将浓硝酸分别放在冷暗处和强光下,发现强光下的浓硝酸分解得快 |
D. |
两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加点二氧化锰,同时加热,放出氧气的快慢不同 |
(16分)某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置(图3)。
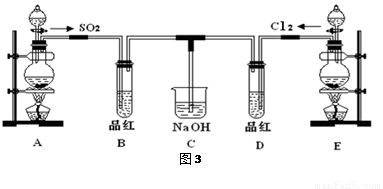
(1)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:________________________________,D:____________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:________________________________,D:____________________________。
(2)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)______________________________ 。
(3)装置E中用MnO2和浓盐酸反应制得Cl2,若反应生成的Cl2体积为2.24L(标准状况),则被氧化的HCl为 mol。
(4)实验结束后,有同学认为装置C中可能含有SO32-、SO42-、Cl-、OH-等阴离子,请填写检验其中SO42-和SO32-的实验报告。
限选试剂:2 mol·L-1 HCl;1 mol·L-1 H2SO4;l mol·L-1 BaCl2;l mol·L-1MgCl2
1 mol·L-1 HNO3;0.1 mol·L-1 AgNO3;新制饱和氯水。
|
编号 |
实验操作 |
预期现象和结论 |
|
步骤① |
取少量待测液于试管中,滴入 至过量
|
,证明待测液中含SO32-。 |
|
步骤② |
在步骤①的溶液中滴入少量
|
, 证明待测液中含SO42-。 |