题目内容
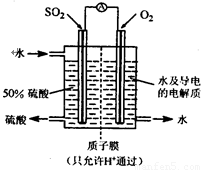
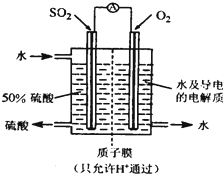
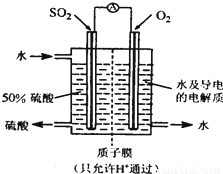
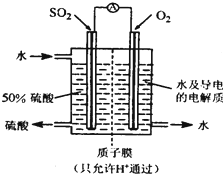 一种新型的利用电化学反应原理来制备硫酸的方法已 经问世,其装置如图所示,电极为多孔的惰性电极,稀硫酸作电解质溶液,电池工作时,一极通入SO2气体,另一极通入O2.下列有关叙述正确的是( )
一种新型的利用电化学反应原理来制备硫酸的方法已 经问世,其装置如图所示,电极为多孔的惰性电极,稀硫酸作电解质溶液,电池工作时,一极通入SO2气体,另一极通入O2.下列有关叙述正确的是( )分析:该装置是原电池,负极上的物质失电子发生氧化反应,正极上的物质得电子发生还原反应,原电池放电时,电解质溶液中的阳离子向正极移动,阴离子向负极移动.
解答:解:A.通入氧气的电极上,氧气得电子发生还原反应,所以通入氧气的电极是正极,故A错误;
B.通入氧气的电极是正极,正极上氧气得电子和氢离子反应生成水,电极反应式为:O2+4e-+4H+=2H2O,故B错误;
C.原电池放电时,氢离子向正极移动,故C错误;
D.负极上,二氧化硫失电子和水反应生成硫酸,电极反应式为:2SO2-4e-+4H2O=2SO42-+8H+,故D正确;
故选D.
B.通入氧气的电极是正极,正极上氧气得电子和氢离子反应生成水,电极反应式为:O2+4e-+4H+=2H2O,故B错误;
C.原电池放电时,氢离子向正极移动,故C错误;
D.负极上,二氧化硫失电子和水反应生成硫酸,电极反应式为:2SO2-4e-+4H2O=2SO42-+8H+,故D正确;
故选D.
点评:本题考查了原电池原理,注意原电池放电时,溶液中阴阳离子的移动方向,为易错点.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
一种新型的利用电化学反应原理来制备硫酸的方法已经问世,其装置如图所示,电极为多孔的惰性电极,稀硫酸作电解质溶液,电池工作时,一极通入SO2气体,另一极通入O2。下列有关叙述正确的是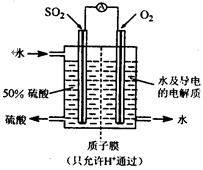
| A.通入O2的电极为负极 |
| B.正极反应式为:O2+4e-+2H2O=4OH- |
| C.电池工作时H+移向负极 |
| D.负极反应式为:2SO2 - 4e- + 4H2O = 2SO42- + 8H+ |