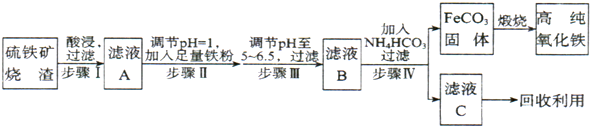
��Ŀ����
ij�Լ��������Ļ�ѧ�Լ�FeCl3��6H2O�����ҹ涨�����Ʒ��������������99.0%������Ʒ��������������98.0%���ֳ�ȡ0.500g��Ʒ��������ˮ����������Һ�м���������ʹ֮�ữ�������������KI��Һ��ַ�Ӧ(2Fe3++2I-=2Fe2++I2)�������0.100mol/L��Na2S2O3����Һ�ζ���Na2S2O3��I2��Ӧ�Ļ�ѧ����ʽΪ��I2+2Na2S2O3=2NaI+Na2S4O6���ζ����յ�ʱ��ȥNa2S2O318.17mL����ͨ������˵������Ʒ������һ����Ʒ��
�𰸣�
������
������
��������Ϊ98.3%������Ʒ �ù�ϵʽ����֮������Ʒ��FeCl3��6H2OΪx(mol)���ɷ�Ӧ����ʽ�����¹�ϵʽ�� 2Fe3+��I2��2Na2S2O3 2mol 2mol xmol 0.1´18.17´10-3mol �� x=1.817´10-3(mol)����
����������
|

��ϰ��ϵ�д�
 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
�����Ŀ