题目内容
“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
___ C+ ___ KMnO4+ ____ H2SO4→____CO2↑+ ____MnSO4 + ____K2SO4+ ____H2O
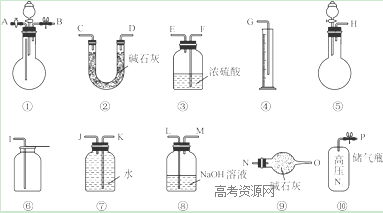
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)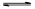 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
①实验2条件下平衡常数K= 。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值______(填具体值或取值范围)。
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时V正 V逆(填“<” ,“>” ,“=”)。
(3)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:____________
(4)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。常温下,向10 mL 0.01 mol·L-1 H2C2O4溶液中滴加10mL 0.01mol·L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系 ;
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。
CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为1×10-4mo1/L ,则生成沉淀所需CaCl2溶液的最小浓度为 mo1/L 。
(共15分)
(1) 5、4、6、5、4、2、6(2分)
(2)①1/6或0.17(2分) ②<1 (填0<a/b<1亦可)(2分) ③< (2分)
(3)CH3OH(l)+ O2(g) = CO(g) + 2H2O(l) ΔH=﹣442.8 kJ∕mol (3分)
(聚集状态没注明不得分,未配平不得分)
(4)c(Na+)> c(HC2O4-)> c(H+)> c(C2O42-) > c(OH-)(2分);(5)1.12×10— 4mo1/L (2分)
解析试题分析:
(1)反应中C→CO2,碳元素化合价由0价升高为+4价,共升高4价,KMnO4→MnSO4,Mn元素化合价由+7价降低为+2价,共降低5价,化合价升降最小公倍数为20,故C的系数为5,故KMnO4系数为4,结合原子守恒配平后方程式为:5C+4KMnO4+6H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O
(2)①、平衡时CO的物质的量为1.6mol,则:
CO(g)+H2O(g)=CO2(g)+H2(g),
开始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
该反应前后气体体积不变,故利用物质的量代替浓度计算平衡常数,故900℃时该反应平衡常数k= =0.17,
=0.17,
②、由于CO与H2的化学计量数相等都为1,所以当两者物质的量相等时二者转化率相等。要使CO转化率大于H2的转化率,则增大H2的物质的量,即a/b的值小于1,
③、由①900℃时,该反应的平衡常数为0.17,实验4,在900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时浓度商Qc= =1,大于平衡常数0.17,故反应向逆反应进行,所以V正<V逆,
=1,大于平衡常数0.17,故反应向逆反应进行,所以V正<V逆,
(3)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(l)△H=-44.0kJ/mol
依据盖斯定律①-②+③×4得:2CH3OH(l)+2O2(g)="2CO" (g)+4H2O(l)△H=-885.6KJ/mol;
即CH3OH(l)+O2(g)="CO" (g)+2H2O(l)△H=-442.8KJ/mol;
(4)向10mL 0.01mol?L-1 H2C2O4溶液中滴加10mL 0.01mol?L-1 NaOH溶液,二者恰好反应,所得溶液为NaHC2O4溶液,在该溶液中,直接电离出的Na+和HC2O4-浓度最大,NaHC2O4溶液显酸性,说明HC2O4-的电离程度大于水解,所以c(Na+)>c(HC2O4-),c(H+)>c(OH-),溶液中水电离生成氢离子,故c(H+)>c(C2O42-),溶液呈酸,电离产生的c(C2O42-)原大于c(OH-),溶液中离子浓度c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-),
(5)Na2CO3溶液的浓度为1×10-4mo1/L,等体积混合后溶液中
c(CO32-)= ×1×10-4mo1/L=5×10-5mo1/L,根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,钙离子最小浓度c(Ca2+)=
×1×10-4mo1/L=5×10-5mo1/L,根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,钙离子最小浓度c(Ca2+)= mol/L=5.6×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×5.6×10-5mol/L=1.12×10-4mol/L。
mol/L=5.6×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×5.6×10-5mol/L=1.12×10-4mol/L。
考点定位:本题考查氧化还原反应配平、平衡常数的计算与运用、热化学方程式书写、离子浓度大小比较、溶度积的有关计算等,题目综合性较大,是对学生能力的考查,难度中等,(5)中计算为易错点,溶液忽略混合后溶液的浓度发生变化。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案Ⅰ.卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性
质,查阅资料并进行实验。查阅资料如下:
① BrO3- + 6I- + 6H+ = 3I2 + Br-+ 3H2O ② 2BrO3- + I2 = 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2 + 3H2O ④ 2IO3- + 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
实验如下:
| 步骤 | 现象 |
| ⅰ.向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 | 随着KBrO3溶液滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
| ⅱ.继续向上述溶液中滴入KBrO3溶液 | 溶液的蓝色逐渐褪去 |
请回答:
(1)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是 ;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是 。
(2)若用y表示锥形瓶中含碘物质的物质的量 ,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。

Ⅱ.过碳酸钠中含有少量过氧化钠,甲、乙两位同学各称取一定质量的该样品,并用如下图所示仪器测定样品的纯度。仪器的连接顺序:
甲同学:⑤—⑧—③—⑦—④; 乙同学:⑤—③—②。
已知:过碳酸钠(Na2CO4)、过氧化钠分别跟足量稀硫酸反应的化学方程式如下:
2Na2CO4+2H2SO4=2Na2SO4+2CO2↑+O2↑+2H2O;
2Na2O2+2H2SO4=2Na2SO4+O2↑+2H2O。
(1)甲同学想通过实验测得的数据是____________,他选用的装置________(填序号)是没有必要的。
(2)乙同学想通过实验测得的数据是________________。有人认为按他测得的数据计算出的实验结果可能偏高,原因是________________; 为了测得准确的实验数据,请你将乙同学的实验设计进行改进,写出你所选用仪器的连接顺序(每种仪器最多使用一次,也可以不用):________________(填序号)。

 AsO43-+2I-+ 2H2O,在较强酸性时,上述氧化还原反应向____进行(填:“正反应”或“逆反应”);强碱性时,是否有利H3As3还原I2?为什么?_______________________________________。
AsO43-+2I-+ 2H2O,在较强酸性时,上述氧化还原反应向____进行(填:“正反应”或“逆反应”);强碱性时,是否有利H3As3还原I2?为什么?_______________________________________。

 已知: ,假设测定过程中没有其他反应。根据上述数据,该产品中PCl3的质量分数为 。
已知: ,假设测定过程中没有其他反应。根据上述数据,该产品中PCl3的质量分数为 。