题目内容
16.按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上.(1)CH3CH2CH2COOH羧酸,(2)CH3CH2CH2CH2-Cl卤代烃,(3)HCOOC2H5酯类,(4)CH3CHO醛类,(5)CH3CH2CH=CHCH3烯烃,(6)
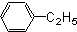 芳香烃,(7)
芳香烃,(7) 酚,(8)
酚,(8)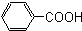 芳香酸.
芳香酸.
分析 根据烃的衍生物的官能团可确定有机物的种类,常见有机物有烯烃、炔烃、醇、酚、醛、酸、酯等,结合有机物的结构简式判断有机物的种类.
解答 解:(1)CH3CH2CH2COOH:官能团为羧基,属于羧酸;
(2)CH3CH2CH2CH2-Cl:官能团为氯原子,故属于卤代烃;
(3)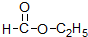 :分子中含有酯基,属于酯;
:分子中含有酯基,属于酯;
(4)CH3CHO:官能团为醛基,故属于醛;
(5)CH3CH2CH=CHCH3:此物质是官能团为碳碳双键的烃类,故属于烯烃;
(6)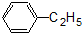 :该有机物为乙苯,分子中不含官能团,含有苯环,属于芳香烃;
:该有机物为乙苯,分子中不含官能团,含有苯环,属于芳香烃;
(7) :官能团为羟基,属于酚;
:官能团为羟基,属于酚;
(8)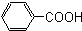 :由于含苯环,且官能团为羧基,属于芳香酸;
:由于含苯环,且官能团为羧基,属于芳香酸;
故答案为:(1)羧酸,(2)卤代烃,(3)酯,(4)醛,(5)烯烃,(6)芳香烃,(7)酚,(8)芳香酸.
点评 本题考查有机物的官能团及其结构,题目难度不大,注意把握有机物的结构特点和官能团的结构和性质,学习中注意把握有机物的类别和性质.

练习册系列答案
相关题目
6.已知1~18号元素的离子W3+、X+、Y2-、Z-都具有相同的电子层结构,下列关系正确的是( )
| A. | 元素原子失电子能力:X>W | B. | 离子的还原性:Z->Y2- | ||
| C. | 氢化物的稳定性:H2Y>HZ | D. | 原子半径:X<W |
7.下列说法正确的是( )
| A. | 明矾溶于水产生Al(OH)3 胶体,离子方程式可表示为:Al3++3H2O═Al(OH)3↓+3H+ | |
| B. | 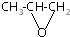 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物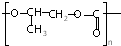 ,该反应符合绿色化学的原则 ,该反应符合绿色化学的原则 | |
| C. | 用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 | |
| D. | 聚氯乙烯塑料制品可用于食品的包装 |
11.在反应:C+CO2 ?2CO中,可使反应速率增大的措施是( )
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤用等量炭粉代替焦炭.
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤用等量炭粉代替焦炭.
| A. | ①②③ | B. | ②③④⑤ | C. | ①②③⑤ | D. | ②③④ |
1.下列溶液肯定呈酸性的是( )
| A. | 含有 H+离子的溶液 | B. | 酚酞显无色的溶液 | ||
| C. | c(OH-)<c(H+)的溶液 | D. | pH 小于 7 的溶液 |
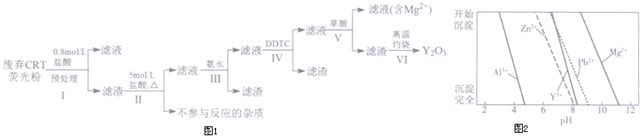
6.稀土是一种不可再生的战略性资源,被广泛应用于电子信息、国防军工等多个领域.一种从废弃阴极射线管(CRT)荧光粉中提取稀土元素钇(Y)的工艺流程如图1:
已知:①废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)如表一所示;
②不同离子沉淀的pH如图2所示.
(1)步骤I中进行原料预处理的目的为除去ZnO和Al2O3;富集稀土元素;降低后续耗酸量.
(2)步骤Ⅱ中有黄绿色气体产生,该反应的化学方程式为PbO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O.
(3)步骤Ⅲ中发生的主要反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(4)步骤Ⅳ中除杂试剂DDTC除去的杂质离子有Zn2+、Pb2+,其不能通过直接加碱的方法除去,原因为Zn2+、Pb2+与Y3+沉淀的pH相近,三者因同时沉淀而无法分离.
(5)步骤V中Y3+沉淀完全时,需保证滴加草酸后的溶液中c(C2O42-)不低于2.0×10-6mol/L.
(已知:当离子浓度小于10-5mol/L时,沉淀就达完全;K甲[Y2(C2O4)3]=8.0×10-28
(6)步骤Ⅵ中草酸钇隔绝空气加热可以得到Y2O3,该反应的化学方程式为Y2(C2O4)3$\frac{\underline{\;\;△\;\;}}{\;}$Y2O3+3CO↑+3CO2↑.
已知:①废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)如表一所示;
②不同离子沉淀的pH如图2所示.
| 成分 含量/% 阶段 | Y2O3 | ZnO | Al2O3 | PbO2 | MgO |
| 预处理前 | 24.28 | 41.82 | 7.81 | 1.67 | 0.19 |
| 预处理后 | 68.51 | 5.42 | 4.33 | 5.43 | 0.50 |
(2)步骤Ⅱ中有黄绿色气体产生,该反应的化学方程式为PbO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O.
(3)步骤Ⅲ中发生的主要反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(4)步骤Ⅳ中除杂试剂DDTC除去的杂质离子有Zn2+、Pb2+,其不能通过直接加碱的方法除去,原因为Zn2+、Pb2+与Y3+沉淀的pH相近,三者因同时沉淀而无法分离.
(5)步骤V中Y3+沉淀完全时,需保证滴加草酸后的溶液中c(C2O42-)不低于2.0×10-6mol/L.
(已知:当离子浓度小于10-5mol/L时,沉淀就达完全;K甲[Y2(C2O4)3]=8.0×10-28
(6)步骤Ⅵ中草酸钇隔绝空气加热可以得到Y2O3,该反应的化学方程式为Y2(C2O4)3$\frac{\underline{\;\;△\;\;}}{\;}$Y2O3+3CO↑+3CO2↑.

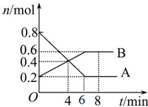 某温度时,在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示.
某温度时,在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示.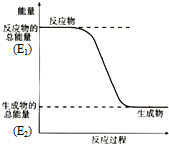 某元素的原子最外层电子数是次外层电子数的两倍,该元素是碳;它在元素周期表中的位置是第二周期第ⅣA族;该元素和氢元素组成的某种有机物是“西气东输”中“气”的主要成分,这种有机物的电子式为
某元素的原子最外层电子数是次外层电子数的两倍,该元素是碳;它在元素周期表中的位置是第二周期第ⅣA族;该元素和氢元素组成的某种有机物是“西气东输”中“气”的主要成分,这种有机物的电子式为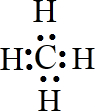 ;结构式
;结构式 ;空间构型:正四面体.这种化合物中碳元素的质量分数为75%.该物质在氧气中充分燃烧的反应方程式:CH4+2O2 $\stackrel{点燃}{→}$CO2+2H2O.一定量的该气体燃烧过程的能量变化如图所示,从图中可以读出E1>E2(填写“>”或者“<”),该反应放热(填写“放出”或者“吸收”)能量.该物质与Cl2反应方程式为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl(只写出第一步反应),该反应类型为取代反应.
;空间构型:正四面体.这种化合物中碳元素的质量分数为75%.该物质在氧气中充分燃烧的反应方程式:CH4+2O2 $\stackrel{点燃}{→}$CO2+2H2O.一定量的该气体燃烧过程的能量变化如图所示,从图中可以读出E1>E2(填写“>”或者“<”),该反应放热(填写“放出”或者“吸收”)能量.该物质与Cl2反应方程式为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl(只写出第一步反应),该反应类型为取代反应.