题目内容
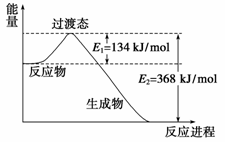
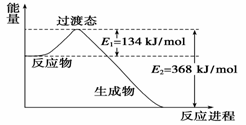
(1)下图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: 。
(2))依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=C02(g) △H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599kJ·mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变:
△H=_____ 。
(3)2.3 g某液态有机物和一定量的氧气混合点燃,恰好完全燃烧,生成2.7 g水和2.24 L CO2(标准状况),并放出68.35 kJ热量,则该反应的热化学方程式为:
。
(1)NO2(g)+CO(g)===CO2(g)+NO(g) ΔH=-234 kJ/mol
(2)226.7kJ·mol-1
(3)C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(l) ΔH=-1367 kJ/mol

练习册系列答案
相关题目