题目内容
硫酸在下列用途或反应中所表现的性质(用字母填在横线上)。
① 浓硫酸可用作气体干燥剂 ;
② 往晶体硫酸铜中加浓硫酸,晶体变白 ;
③ 浓硫酸与铜反应 ;
④ 运用铁制槽车和铝制槽车运输浓硫酸 ;
⑤ 浓硫酸使润湿蓝色石蕊试纸先变红后又变黑 。
| A.难挥发性 | B.强酸性 | C.吸水性 | D.脱水性 E.强氧化性 |
② 往晶体硫酸铜中加浓硫酸,晶体变白 ;
③ 浓硫酸与铜反应 ;
④ 运用铁制槽车和铝制槽车运输浓硫酸 ;
⑤ 浓硫酸使润湿蓝色石蕊试纸先变红后又变黑 。
(5分)① C ② C ③ BE ④ E ⑤ BD(每空1分)
试题分析:①浓硫酸具有吸水性,所以浓硫酸可用作气体干燥剂,答案选C。
② 同样由于浓硫酸具有吸水性,所以往晶体硫酸铜中加浓硫酸,晶体变白,答案选C。
③根据反应式Cu+2H2SO4(浓)
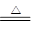 CuSO4+2H2O+SO2↑可知,在该反应中浓硫酸表现的是酸性和强氧化性,答案选BE。
CuSO4+2H2O+SO2↑可知,在该反应中浓硫酸表现的是酸性和强氧化性,答案选BE。④常温下铝或铁在浓硫酸中发生钝化,所以可以运用铁制槽车和铝制槽车运输浓硫酸,表现的是浓硫酸的强氧化性,答案选E。
⑤浓硫酸具有酸性和脱水性,所以浓硫酸使润湿蓝色石蕊试纸先变红后又变黑,答案选BD。
点评:该题是高考中的常见考点,属于基础性试题的考查,试题基础性强,主要是考查学生对浓硫酸性质的熟悉掌握程度,以及灵活运用浓硫酸的性质解决实际问题的能力,有利于培养学生的逻辑推理能力,提高学生的应试能力。

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
 下列说法正确的是
下列说法正确的是 →MnO2
→MnO2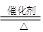 4NO + 6H2O ,其中作为还原剂的物质是 (填化学式);若反应中生成了0.2 mol NO,则转移 mol电子,
4NO + 6H2O ,其中作为还原剂的物质是 (填化学式);若反应中生成了0.2 mol NO,则转移 mol电子,