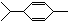题目内容
11.下列有关丙烷的叙述不正确的是( )| A. | 是直链烃,但分子中碳原子不在一条直线上 | |
| B. | 在光照条件下能够与氯气发生取代反应 | |
| C. | 丙烷比其同分异构体丁烷易汽化,耗氧量少 | |
| D. | 燃烧时主要是将化学能转变为热能和光能 |
分析 A、烷烃分子中有多个碳原子应呈锯齿形,丙烷呈角形;
B、丙烷等烷烃在光照的条件下可以和氯气发生取代反应;
C、根据丙烷分子式计算耗氧量,烷烃中碳个数越多沸点越高,分子式相同,结构不同的属于同分异构体;
D、从燃烧的定义来分析能量转化.
解答 解:A、烷烃分子中有多个碳原子应呈锯齿形,丙烷呈角形,碳原子不在一条直线上,故A正确;
B、丙烷等烷烃在光照的条件下可以和氯气发生取代反应,故B正确;
C、烷烃中碳个数越多沸点越高,丙烷分子中碳原子数小于丁烷,故丁烷沸点高,更易液化,丙烷分子式为C3H8,1mol丙烷耗氧量为碳和氢耗氧量之和:(3+$\frac{8}{4}$)mol=5mol,1mol丁烷耗氧量为:4+$\frac{10}{4}$=6.5mol,丁烷耗氧量大,但丙烷与丁烷不是同分异构体,故C错误;
D、所有发光发热的氧化还原反应称为燃烧,因此燃烧主要是把化学能转化为热能和光能,故D正确,故选C.
点评 本题主要考查丙烷的结构与性质等,难度较小,注意基础知识的积累掌握,注意从燃烧的定义来分析能量转化.

练习册系列答案
相关题目
1.分类法在化学学科的发展中起到了非常重要的作用,下列分类标准不合理的是( )
| A. | 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 | |
| B. | 根据反应中是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据是否含氧元素,将物质分为氧化剂和还原剂 | |
| D. | 根据水溶液或熔融状态是否能够导电,将化合物分为电解质和非电解质 |
2.某课外兴趣小组对H2O2的分解速率做了如下实验探究:
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用l0mL H2O2制取150mL O2所需的时问(s)
①验证影响反应速率的因素时要考试控制变量.取相同浓度的H2O2进行实验,上表反应条件中考虑控制单因子变量的是温度、浓度、催化剂.
②对照反应条件a和b,可以说明催化剂 因素对过氧化氢分解的速率有影响,该影响可具体表述为催化剂加快分解速率.
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试.测试结果加下.
①写出加入MnO2后H2O2发生反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②上述实验中,使用粉末状催化剂和块状催化剂所得过氧化氢分解反应的反应速率之比为10:1.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用l0mL H2O2制取150mL O2所需的时问(s)
| 浓度 时间(s) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热(t1℃) | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热(t2℃) | 360(a) | 480 | 540 | 720 |
| MnO2催化剂、加热(t2℃) | 10(b) | 25 | 60 | 120 |
②对照反应条件a和b,可以说明催化剂 因素对过氧化氢分解的速率有影响,该影响可具体表述为催化剂加快分解速率.
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试.测试结果加下.
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3min |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30min |
②上述实验中,使用粉末状催化剂和块状催化剂所得过氧化氢分解反应的反应速率之比为10:1.
6.某油脂样品跟氢氧化钠溶液共热后经酸化得到3种有机物,原样品最多可能含有的三羧酸甘油酯有( )
| A. | 3种 | B. | 6种 | C. | 7种 | D. | 8种 |
16.常温下,盐酸和一元碱MOH溶液等体积混合(忽略体积变化),实验数据如下表:
下列判断正确的是( )
| 实验编号 | 起始浓度/(mol•L-1) | 反应后溶液的pH | |
| c(HCl) | c(MOH) | ||
| ① | 0.1 | 0.1 | 5 |
| ② | 0.2 | x | 7 |
| ③ | 0.1 | 0.2 | 10 |
| ④ | 0.2 | 0.1 | y |
| A. | 实验①反应后的溶液中:c(MOH)约为1×10-5 mol•L-1 | |
| B. | 实验②反应后的溶液中:c(MOH)>c(M+)=c(Cl-)>c(H+)=c(OH-) | |
| C. | 实验③反应后的溶液中:c(M+)+c(H+)=c(OH-)+c(MOH) | |
| D. | 实验④反应后的溶液中:c(H+)-c(OH-)-c(MOH)=0.05mol•L-1 |
16.下列说法正确的是( )
| A. | 由于水中存在氢键,所以水很稳定 | |
| B. | 能与酸反应生成盐和水的氧化物一定是碱性氧化物 | |
| C. | Na2O2中既含有离子键,又含有非极性键 | |
| D. | 由于C═O键是极性键,所以CO2是极性分子 |
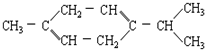 还可以简写为
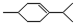
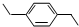
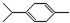
还可以简写为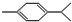 ,下列有机物中,与上述有机物互为同分异构体的是( )
,下列有机物中,与上述有机物互为同分异构体的是( )