题目内容
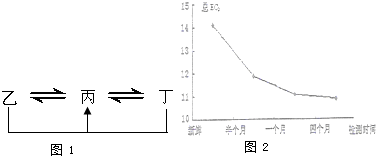
(8分) A、B、C、D、E、F六种物质的相互转化关系如 下图所示(反应条件未标出),其中反应①是置换反应。
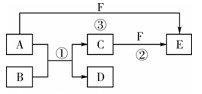
(1)若A是常见的金属单质,D、F是气态单质,反应① 在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是_____________________________。
(2)若B、C、F都是气态单质,且B有毒,③的反应中还有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则A、D反应产物的电子式是_________________,反应③的化学方程式是______________________________。
(3)若A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是 。
列举物质B的一个重要用途 。
(8分)(1)2Fe2++Cl2=2Fe3++2Cl-(2分)
(2)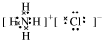 (1分) 4NH3+5O2
(1分) 4NH3+5O2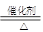 4NO+6H2O (2分)
4NO+6H2O (2分)
(3)2C+SiO2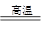 Si+2CO↑(2分) 光导纤维(1分)
Si+2CO↑(2分) 光导纤维(1分)
【解析】
试题分析:(1)若A是常见的金属单质,则根据图中的转化可知,A应该是变价的金属,因此A是铁,B是盐酸,D是氢气,C是氯化亚铁,F是氯气,E是氯化铁,所以反应②(在水溶液中进行)的离子方程式是2Fe2++Cl2=2Fe3++2Cl-。
(2)反应②需要放电才能发生,所以C是氮气,F是氧气E是NO,则A是氨气,B是氯气,D是氯化氢或氯化铵。A、D相遇有白烟生成,所以D是氯化氢,生成物氯化铵是离子化合物,电子式是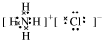 。其中反应③是氨气的催化氧化,方程式是4NH3+5O2
。其中反应③是氨气的催化氧化,方程式是4NH3+5O2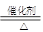 4NO+6H2O。
4NO+6H2O。
(3)A、D所含元素同主族,则符合条件是碳和硅、氧气和S。又因为A、F所含元素同周期,所以A是碳、B是二氧化硅、C是CO、D是硅、E是CO2、F是氧气,则反应①的化学方程式是2C+SiO2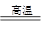 Si+2CO↑。二氧化硅的主要用途是光导纤维。
Si+2CO↑。二氧化硅的主要用途是光导纤维。
考点:考查根据框图进行的有关判断
点评:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合。它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法。解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。

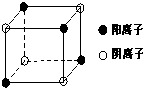 [化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.
[化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.