题目内容
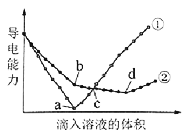
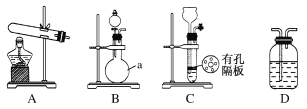
【题目】在25 mL 0.1 mol/L的NaOH溶液中逐滴加入0.2 mol/L醋酸溶液,曲线如图所示,有关粒子的浓度关系正确的是
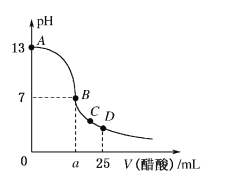
A.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
【答案】CD
【解析】对于选项A,找一个特殊点,当NaOH溶液中只滴入少量醋酸时,这时碱远远过量,溶液中只有少量的CH3COONa,因此关系为c(Na+)>c(OH-)>c(CH3COO-)>c(H+),A项错;对于选项B,在B点时,溶液的pH恰好为7,根据电荷守恒有:c(Na+)=c(CH3COO-)>c(OH-)=c(H+),B项错;C、D项正确。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目